题目内容
(26分)分析比较前后两个量的关系(用<或>回答),并给出合理的解释:
(1)元素的第一电离能:S____P,理由是:___________________________________。
(2)物质的沸点:
①SiCl4_____ SiF4,理由是:_____________________________________________。
②HCl______HF,理由是:_________________________________________。
(3)晶体的熔点:
①SiO2_____ CO2,理由是:_______________________________________。
②MgCl2______MgO,理由是:____________________________________。
(4)原子半径:O_____Na,O2—_____Na+,理由是:_____________________________________
(1)元素的第一电离能:S____P,理由是:___________________________________。
(2)物质的沸点:
①SiCl4_____ SiF4,理由是:_____________________________________________。
②HCl______HF,理由是:_________________________________________。
(3)晶体的熔点:
①SiO2_____ CO2,理由是:_______________________________________。
②MgCl2______MgO,理由是:____________________________________。
(4)原子半径:O_____Na,O2—_____Na+,理由是:_____________________________________
(1)< 由于P原子的3p轨道电子处于半充满状态,稳定性强,所以第一电离能大于S原子的第一电离能。
(2)①> 由于SiCl4和SiF4的结构、性质相似,且二者形成的晶体是分子晶体,物质的沸点和分子间作用力大小有关系。由于相对分子质量越大,分子间作用力越大,所以前者的沸点高于后者。
②< 由于HF分子中含有氢键,所以氟化氢的沸点高于氯化氢的沸点。
(3)①> 由于SiO2和 CO2形成的晶体分别是原子晶体和分子晶体,所以前者的熔点高于后者。
②< 由于MgCl2和MgO形成的晶体都是离子晶体,形成离子晶体的离子半径越小,电荷数越多,晶格能越大,熔点就越高。氧离子半径小于氯离子半径,所以前者的熔点低于后者。
(4)< > 由于同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐最大,所以氧原子半径小于钠原子半径;又因为核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,因此O2—半径大于Na+半径。
(2)①> 由于SiCl4和SiF4的结构、性质相似,且二者形成的晶体是分子晶体,物质的沸点和分子间作用力大小有关系。由于相对分子质量越大,分子间作用力越大,所以前者的沸点高于后者。
②< 由于HF分子中含有氢键,所以氟化氢的沸点高于氯化氢的沸点。
(3)①> 由于SiO2和 CO2形成的晶体分别是原子晶体和分子晶体,所以前者的熔点高于后者。
②< 由于MgCl2和MgO形成的晶体都是离子晶体,形成离子晶体的离子半径越小,电荷数越多,晶格能越大,熔点就越高。氧离子半径小于氯离子半径,所以前者的熔点低于后者。
(4)< > 由于同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐最大,所以氧原子半径小于钠原子半径;又因为核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,因此O2—半径大于Na+半径。
(1)非金属性越强,电负性越大,但由于P原子的3p轨道电子处于半充满状态,稳定性强,所以第一电离能大于S原子的第一电离能。
(2)①由于SiCl4和SiF4的结构、性质相似,且二者形成的晶体是分子晶体,物质的沸点和分子间作用力大小有关系。由于相对分子质量越大,分子间作用力越大,所以前者的沸点高于后者。
②由于HF分子中含有氢键,所以氟化氢的沸点高于氯化氢的沸点。
(3)①由于SiO2和 CO2形成的晶体分别是原子晶体和分子晶体,所以前者的熔点高于后者。
②由于MgCl2和MgO形成的晶体都是离子晶体,形成离子晶体的离子半径越小,电荷数越多,晶格能越大,熔点就越高。氧离子半径小于氯离子半径,所以前者的熔点低于后者。
(4)由于同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐最大,所以氧原子半径小于钠原子半径;又因为核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,因此O2—半径大于Na+半径。
(2)①由于SiCl4和SiF4的结构、性质相似,且二者形成的晶体是分子晶体,物质的沸点和分子间作用力大小有关系。由于相对分子质量越大,分子间作用力越大,所以前者的沸点高于后者。
②由于HF分子中含有氢键,所以氟化氢的沸点高于氯化氢的沸点。
(3)①由于SiO2和 CO2形成的晶体分别是原子晶体和分子晶体,所以前者的熔点高于后者。
②由于MgCl2和MgO形成的晶体都是离子晶体,形成离子晶体的离子半径越小,电荷数越多,晶格能越大,熔点就越高。氧离子半径小于氯离子半径,所以前者的熔点低于后者。
(4)由于同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐最大,所以氧原子半径小于钠原子半径;又因为核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,因此O2—半径大于Na+半径。

练习册系列答案
相关题目
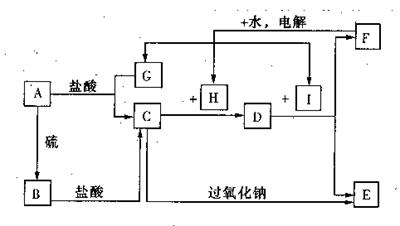
 采取的方法是 。
采取的方法是 。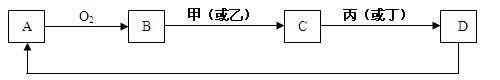
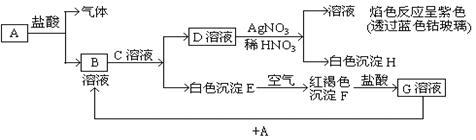
 ;B ; H ;F
;B ; H ;F 