题目内容
【题目】海洋是资源的宝库,具有十分巨大的开发潜力。工业上从海水提取金属镁的流程如下:

回答下列问题:
(1)沉淀剂是________________(填化学式),不选用同类的其他物质的理由是_______________。
(2)下列选项中,涉及的操作包含操作Ⅰ的是___________。
A 实验室从溴水中提取溴单质
B 除去![]() 固体中的少量NaCl
固体中的少量NaCl
C 从![]() 分解产物中获得
分解产物中获得![]()
D 用工业酒精制无水乙醇
(3)在进行步骤Ⅱ时,如果没有加入盐酸,可能产生的杂质是______________(填化学式)。
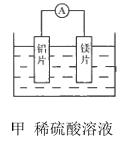
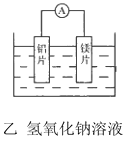
(4)一种模拟工业用![]() 制无水
制无水![]() 的实验室设计如下:
的实验室设计如下:

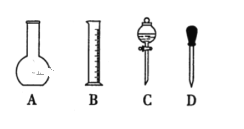
装置A中盛放液体是______________,装置D的作用是____________________________。
(5)步骤Ⅳ发生反应的化学方程式是___________________________________________________。
【答案】Ca(OH)2 Ca(OH)2来源丰富,制造成本低 BC Mg(OH)2或Mg(OH)Cl 浓盐酸 吸收尾气中的HCl,防止空气中的水蒸气进入装置C MgCl2(熔融) ![]() Mg+Cl2↑
Mg+Cl2↑
【解析】
向海水中加入石灰乳,进行沉淀,沉淀出氢氧化镁,再将氢氧化镁与稀盐酸反应生成氯化镁,在酸性条件下对氯化镁溶液蒸发结晶得到氯化镁晶体,在经过洗涤干燥得到无水氯化镁,电解熔融状态的氯化镁即可得到金属镁。
(1)工业流程中的沉淀剂可用Ca(OH)2,Ca(OH)2来源广泛,资源丰富,制造成本低,可直接从海洋的的贝壳(碳酸钙)煅烧后加水即可得到。
答案为:Ca(OH)2;Ca(OH)2来源丰富,制造成本低;
(2)流程中操作Ⅰ为过滤,
A 实验室从溴水中提取溴单质,利用萃取分液操作,故A错误;
B 除去![]() 固体中的少量NaCl,利用溶解度不同,用少量热水溶解后,降温结晶,过滤,故B正确;
固体中的少量NaCl,利用溶解度不同,用少量热水溶解后,降温结晶,过滤,故B正确;
C 从![]() 分解产物中含有锰酸钾和二氧化锰,锰酸钾可溶而二氧化锰不熔,故获得
分解产物中含有锰酸钾和二氧化锰,锰酸钾可溶而二氧化锰不熔,故获得![]() 的方法为溶解、过滤,故C正确;
的方法为溶解、过滤,故C正确;
D 用工业酒精制无水乙醇用蒸馏的方法,故D错误;
答案选BC。
(3)在进行步骤Ⅱ时,如果没有加入盐酸,氯化镁水解产生Mg(OH)2或Mg(OH)Cl,
答案为:Mg(OH)2或Mg(OH)Cl
(4)该装置利用氯化氢气体在加热的条件下与镁反应制取无水氯化镁,防止氯化镁在溶液中发生水解;装置A中利用难挥发的浓硫酸的脱水性,使浓盐酸挥发出产生氯化氢气体,A盛放液体是浓盐酸,装置D的作用是吸收装置中未反应的氯化氢气体,防止空气中的水分进入C装置;
答案为:浓盐酸;吸收尾气中的HCl,防止空气中的水蒸气进入装置C
(5)制取镁单质,是利用电解熔融氯化镁来生产单质镁。
步骤Ⅳ发生反应的化学方程式是MgCl2(熔融) ![]() Mg+Cl2↑。
Mg+Cl2↑。
答案为:MgCl2(熔融) ![]() Mg+Cl2↑。
Mg+Cl2↑。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】硫铁矿烧渣中含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等,为了充分利用资源,一种利用硫铁矿烧渣制绿矾(
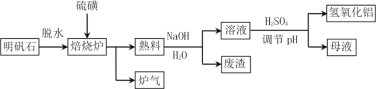
等,为了充分利用资源,一种利用硫铁矿烧渣制绿矾(![]() )的化工流程如下:
)的化工流程如下:
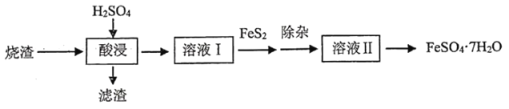
回答下列问题:
(1)酸浸需要使用较浓的硫酸并加热,目的是________________________________,现有![]() ,
,![]() 的硫酸,其物质的量浓度
的硫酸,其物质的量浓度![]() _____________
_____________![]() (保留3位有效数字)。
(保留3位有效数字)。
(2)滤渣除![]() 外,还可能含有__________,溶液Ⅰ需保持
外,还可能含有__________,溶液Ⅰ需保持![]() ,原因是__________。
,原因是__________。
(3)用![]() 还原时,当氧化产物为
还原时,当氧化产物为![]() ,发生主要反应的离子方程式是___________________,检验该反应是否完全发生,所用的试剂是___________________。
,发生主要反应的离子方程式是___________________,检验该反应是否完全发生,所用的试剂是___________________。
(4)除杂时,除去溶液中的![]() ,适宜的物质是_______________。
,适宜的物质是_______________。
A NaOH B H2S C FeS D 氨水
(5)已知![]() ,在不同温度下的溶解度和析出晶体的组成如下表:
,在不同温度下的溶解度和析出晶体的组成如下表:
温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 80 | 90 | |
溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 |
析出晶体 |
|
|
| |||||||
如要获得![]() ,则需对溶液Ⅱ进行的操作是:蒸发浓缩,___________________,过滤,洗涤,干燥。
,则需对溶液Ⅱ进行的操作是:蒸发浓缩,___________________,过滤,洗涤,干燥。