题目内容
【题目】硫铁矿烧渣中含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等,为了充分利用资源,一种利用硫铁矿烧渣制绿矾(
等,为了充分利用资源,一种利用硫铁矿烧渣制绿矾(![]() )的化工流程如下:
)的化工流程如下:
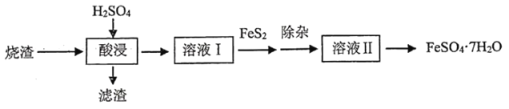
回答下列问题:
(1)酸浸需要使用较浓的硫酸并加热,目的是________________________________,现有![]() ,
,![]() 的硫酸,其物质的量浓度
的硫酸,其物质的量浓度![]() _____________
_____________![]() (保留3位有效数字)。
(保留3位有效数字)。
(2)滤渣除![]() 外,还可能含有__________,溶液Ⅰ需保持
外,还可能含有__________,溶液Ⅰ需保持![]() ,原因是__________。
,原因是__________。
(3)用![]() 还原时,当氧化产物为
还原时,当氧化产物为![]() ,发生主要反应的离子方程式是___________________,检验该反应是否完全发生,所用的试剂是___________________。
,发生主要反应的离子方程式是___________________,检验该反应是否完全发生,所用的试剂是___________________。
(4)除杂时,除去溶液中的![]() ,适宜的物质是_______________。
,适宜的物质是_______________。
A NaOH B H2S C FeS D 氨水
(5)已知![]() ,在不同温度下的溶解度和析出晶体的组成如下表:
,在不同温度下的溶解度和析出晶体的组成如下表:
温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 80 | 90 | |
溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 |
析出晶体 |
|
|
| |||||||
如要获得![]() ,则需对溶液Ⅱ进行的操作是:蒸发浓缩,___________________,过滤,洗涤,干燥。
,则需对溶液Ⅱ进行的操作是:蒸发浓缩,___________________,过滤,洗涤,干燥。
【答案】加快反应速率 11.4 CaSO4 抑制Fe3+水解 14Fe3++FeS2+8H2O===15Fe2++2 SO42-+16H+ KSCN溶液 BC 冷却至57℃结晶
【解析】
硫铁矿烧渣加入硫酸酸浸,得到滤渣为SiO2,滤液中含有三价铁离子、铝离子、钙离子、硫酸根等,加入活化硫铁矿还原得到滤液含有硫酸亚铁、硫酸铝,调节溶液pH5.2~6.5之间可除去铝离子,过滤、蒸发浓缩、冷却结晶得到FeSO47H2O晶体。
(1)为加快酸浸的速度可增大硫酸的浓度,还可以加热,升高温度,还可以把矿渣粉碎,
酸浸需要使用较浓的硫酸并加热,现有![]() ,
,![]() 的硫酸,其物质的量浓度
的硫酸,其物质的量浓度![]()
![]() =11.4
=11.4![]() (保留3位有效数字)。
(保留3位有效数字)。
答案为:11.4;
(2)酸浸过程中,硫酸一定是过量的,滤液中会含有硫酸根离子,由于硫酸钙是微溶物,钙离子可与硫酸根离子结合形成硫酸钙沉淀,滤渣除![]() 外,还可能由硫酸钙。滤液中的三价铁离子易水解,若溶液PH过高,导致三价铁离子生成氢氧化铁沉淀,因此溶液中的PH要保持在0.5到1左右,来抑制铁离子水解;
外,还可能由硫酸钙。滤液中的三价铁离子易水解,若溶液PH过高,导致三价铁离子生成氢氧化铁沉淀,因此溶液中的PH要保持在0.5到1左右,来抑制铁离子水解;
答案为:CaSO4;抑制Fe3+水解;
(3)用![]() 还原三价铁离子时,当氧化产物为
还原三价铁离子时,当氧化产物为![]() ,发生主要反应的离子方程式是14Fe3++FeS2+8H2O===15Fe2++2 SO42-+16H+,检验三价铁是否完全被还原,取少量溶液于试管中,只需要向溶液中加入硫氰化钾,若溶液不变色,说明三价铁离子完全被还原为亚铁离子,若有红色出现,说明溶液中还含有三价铁。
,发生主要反应的离子方程式是14Fe3++FeS2+8H2O===15Fe2++2 SO42-+16H+,检验三价铁是否完全被还原,取少量溶液于试管中,只需要向溶液中加入硫氰化钾,若溶液不变色,说明三价铁离子完全被还原为亚铁离子,若有红色出现,说明溶液中还含有三价铁。
答案为:14Fe3++FeS2+8H2O===15Fe2++2 SO42-+16H+ ;KSCN溶液。
(4)除杂时,不能引入新的杂质,还要将杂质离子处理干净,
A. NaOH可以出去铜离子,同时引入了钠离子,故A不符合;
B. H2S可与铜离子反应转化为硫化铜沉淀,还可防止亚铁离子水解,后面制取![]() 晶体蒸发操作又可以除去过量的硫化氢,没有向溶液中引入新杂质,故B符合;
晶体蒸发操作又可以除去过量的硫化氢,没有向溶液中引入新杂质,故B符合;
C FeS既可用于除去铜离子,硫化铜和FeS都不溶于水,不会引入新的杂质,故C符合;
D 氨水可以沉淀铜离子生成氢氧化铜,过量还会使沉淀溶解,同时向溶液中引入铵根离子,故D不符合。
答案为:BC
(5)有表格数据可知,温度高于56.7℃会转化为![]() ,高于70℃转化为
,高于70℃转化为![]() ,温度低于50度,析出晶体产率较低,因此在结晶过程中,蒸发浓缩后,冷却至低于57℃时进行结晶,过滤,洗涤、干燥;
,温度低于50度,析出晶体产率较低,因此在结晶过程中,蒸发浓缩后,冷却至低于57℃时进行结晶,过滤,洗涤、干燥;
答案为:冷却至57℃ 结晶。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案【题目】已知:pKa=-lgKa。25℃时,几种弱酸的pKa值如下表所示。下列说法正确的是
弱酸的化学式 | CH3COOH | HCOOH | H2SO3 |
pKa | 4.74 | 3.74 | 1.90 7.20 |
A. 向Na2SO3溶液中加入过量乙酸,反应生成SO2
B. 25℃时,pH=8的甲酸钠溶液中,c( HCOOH)=9.9×10-7mol·L-1
C. 25℃时,某乙酸溶液pH=a,则等浓度的甲酸pH=a-1
D. 相同温度下,等浓度的 HCOONa溶液比Na2SO3溶液的pH大
【题目】下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 检验KIO3中的碘元素 | 取少量KIO3晶体溶于适量的蒸馏水,再加入硝酸酸化的AgNO3溶液 |
B | 检验石油裂解气中的乙烯 | 将混合气体通入足量酸性KMnO4溶液中 |
C | 比较HClO和CH3COOH的酸性强弱 | 室温下,用pH计测定饱和的NaClO溶液和饱和的 |
D | 硅酸胶体的制备 | 向 |
A.AB.BC.CD.D