题目内容
6.一定温度和压强下,可逆反应CO(g)+H2O(g)?CO2(g)+H2(g)在密闭容器中达到平衡,请回答下列问题:①若增大H2O(g)的浓度,则CO的转化率增大(填“增大”或“减小”)
②若降低温度,平衡向正反应方向移动,则正反应为放热反应(填“放热”或“吸热”);
③若加入催化剂,则平衡A(填字母代号)
A.不移动;B.向正反应方向移动;C.向逆反应方向移动.
分析 ①增大反应物浓度平衡向正反应方向移动B;
②降低温度,平衡向放热反应方向移动;
③催化剂不改变平衡移动.
解答 解:①若增大H2O(g)的浓度,平衡向正反应方向移动,则CO的转化率增大,故答案为:增大;
②若降低温度,降低温度平衡向放热反应方向移动,平衡向正反应方向移动,则正反应为放热反应,故答案为:放热;
③若加入催化剂,催化剂只改变反应速率不改变平衡移动,所以平衡不移动,故选A.
点评 本题考查化学平衡等知识点,熟悉影响化学平衡移动的因素等即可解答,注意:催化剂能同等程度的改变正逆反应速率,所以不影响平衡移动,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、Cl-、NO3-、K+ | |
| B. | 滴入酚酞显红色的溶液中:Na+、Al3+、CO32-、AlO2- | |
| C. | 加入铝粉产生H2的溶液中:Fe2+、Na+、SO42-、ClO- | |
| D. | 0.1mol•L-1 NaHCO3溶液中:Na+、NH4+、SO42-、NO3- |
14.用下列实验装置完成对应的实验,能达到实验目的且合理的是( )
| A. | 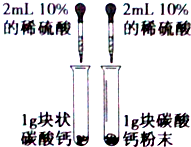 用图装置探究反应物接触面积对反应速率影响 | |
| B. |  用图装置制取并收集少量的NO2气体(不考虑倒吸) | |
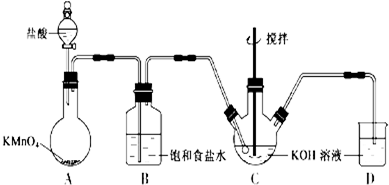
| C. |  用图装置制取并收集少量的氯气 | |
| D. | 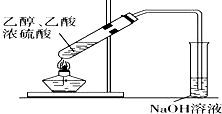 用图装置制取少量乙酸乙酯 |
18.设NA 为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃,1L pH=1的硫酸溶液中含有H+的数为0.2NA | |
| B. | 标准状况下,11.2L NO与11.2L O2混合所含分子数为0.75NA | |
| C. | 在1L的碳酸钠溶液中,若c(CO3 2-)=1mol/L,则Na+个数为2NA | |
| D. | 电镀铜,阳极减少32g,则电路中转移的电子数为NA |
1.用下列实验分离装置进行相应实验,能达到实验目的是( )
| A. |  用图所示装置分离苯和水 | |
| B. |  用图所示装置除去C2H2中含有的少量H2S | |
| C. |  用图所示装置分离NaCl和CaCl2的混合溶液 | |
| D. | 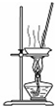 用图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
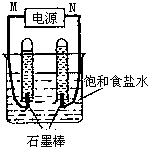 利用反应CO(g)+H2(g)+O2(g)?H2O(g)+CO2(g)设计而成的MCFS燃料电池是一种新型电池.现以该燃料电池为电源,以石墨作电极电解饱和NaCl溶液,反应装置及现象如图所示.则①M应是电源的负极(填“正”或“负”);②该电解反应的化学方程式是2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑;③已知饱和食盐水的体积为1L,一段时间后,测得左侧试管中气体体积为11.2mL(标准状况),若电解前后溶液的体积变化忽略不计,电解后将溶液混合均匀,此时溶液的pH为11.
利用反应CO(g)+H2(g)+O2(g)?H2O(g)+CO2(g)设计而成的MCFS燃料电池是一种新型电池.现以该燃料电池为电源,以石墨作电极电解饱和NaCl溶液,反应装置及现象如图所示.则①M应是电源的负极(填“正”或“负”);②该电解反应的化学方程式是2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑;③已知饱和食盐水的体积为1L,一段时间后,测得左侧试管中气体体积为11.2mL(标准状况),若电解前后溶液的体积变化忽略不计,电解后将溶液混合均匀,此时溶液的pH为11.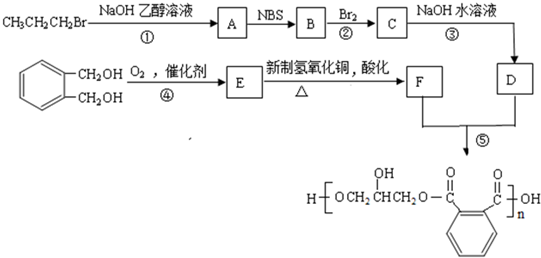
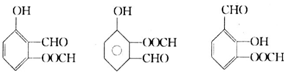 .
. .
.