题目内容
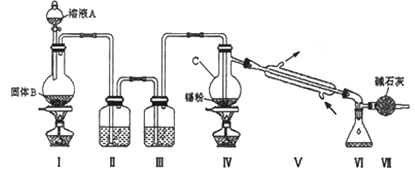
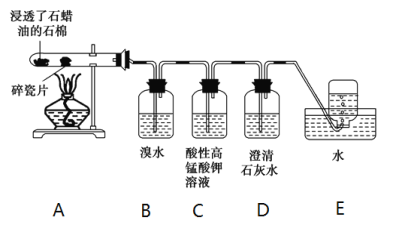
【题目】某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题:
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34 ![]() C8H18+甲,甲
C8H18+甲,甲 ![]() 乙,乙的结构简式为_______。
乙,乙的结构简式为_______。
(2)B装置中发生反应的化学方程式:___________。
(3)C装置中可观察到的现象是________,反应类型是_________。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。本实验能证明这一点的实验现象__________。
(5)乙跟氢气的加成产物与一定量的氯气混合后在光照条件下反应,反应产物共有________。
【答案】CH2= CH2 CH2= CH2+Br2→BrCH2-CH2Br 紫色(或紫红色)褪去 氧化反应 D中的澄清石灰水变浑浊 10
【解析】
(1)依据原子守恒判断甲、乙物质,写出其分子式和结构简式;
(2)乙烯含有碳碳双键,能够与溴发生加成反应;
(3)乙烯具有还原性,能够被酸性高锰酸钾氧化;
(4)二氧化碳与氢氧化钙反应生成碳酸钙沉淀;
(5)结合甲烷与氯气的取代反应分析判断。
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。根据原子守恒,C16H34 ![]() C8H18+甲,所以甲分子式为:C8H16;依据方程式:C8H16
C8H18+甲,所以甲分子式为:C8H16;依据方程式:C8H16 ![]() 4乙,结合原子守恒可知,乙为:C2H4,为乙烯,结构简式为CH2=CH2,故答案为:CH2=CH2;
4乙,结合原子守恒可知,乙为:C2H4,为乙烯,结构简式为CH2=CH2,故答案为:CH2=CH2;
(2)乙烯含有碳碳双键,能够与溴发生加成反应而使溴水褪色,反应的化学方程式为:CH2=CH2+Br2→CH2Br-CH2Br,故答案为:CH2=CH2+Br2→CH2Br-CH2Br;
(3)乙烯具有还原性,能够被酸性高锰酸钾氧化发生氧化反应而使高锰酸钾褪色,故答案为:溶液的紫红色褪去;氧化反应;
(4)乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙反应生成碳酸钙沉淀,溶液变浑浊,因此D中的澄清石灰水变浑浊,可以证明乙烯与酸性高锰酸钾溶液反应产生了二氧化碳,故答案为:D中的澄清石灰水变浑浊;
(5)乙烯跟氢气的加成产物为乙烷,乙烷中含有6个氢原子,生成的有机物有一氯乙烷(1种)、二氯乙烷(2种)、三氯乙烷(2种)、四氯乙烷(2种)、五氯乙烷(1种)、六氯乙烷(1种),还有氯化氢,一共有10种生成物,故答案为:10。

 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案【题目】某地湖盐中含有Ca2+、Mg2+、Fe3+、SO42-等杂质离子,氨碱厂用该地湖盐制取烧碱。其中制得精制食盐水的过程如下:

(1)过程Ⅰ中将粗盐加水溶解需要适当加热,其目的是__________。
(2)过程Ⅱ的目的是除去SO42-,加入的X溶液是__________。
(3)下表是过程Ⅱ、Ⅲ中生成的部分沉淀及其在20℃时的溶解度[g/100gH2O]
CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 | Fe(OH)3 |
2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 | 4.8×10-9 |
①过程Ⅲ中生成的主要沉淀除CaCO3和Fe(OH)3外还有__________。
②过程Ⅳ中调节pH时发生的主要反应的离子方程式为__________。
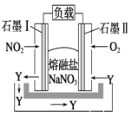
(4)上述精制食盐水中还含有微量的I-、IO3-、NH4+、Ca2+、Mg2+,除去这些离子及进行电解的流程如下:
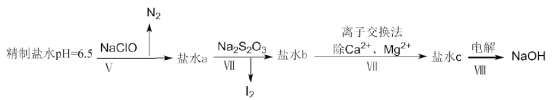
①过程V生成N2的离子方程式为__________。
②过程Ⅳ可以通过控制Na2S2O3的量,将IO3-还原成I2,且盐水b中含有SO42-,该过程中发生氧化还原反应,其中氧化剂和还原剂的物质的量之比为__________。
③在过程Ⅳ中所用的Na2S2O3俗称海波,是一种重要的化工原料。商品海波主要成分是Na2S2O3·5H2O。为了测定其含Na2S2O3·5H2O的纯度,称取8.00g样品,配成250mL溶液,取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500mol·L-1的碘水滴定(发生反应2S2O32-+I2=S4O62-+2I-),下表记录滴定结果:
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
第一次 | 0.30 | 29.12 |
第二次 | 0.36 | 30.56 |
第三次 | 1.10 | 29.88 |
计算样品的纯度为__________。