题目内容
【题目】下列说法不正确的是
A.镀锡的铁片镀层破损后,腐蚀速率加快
B.Fe在食盐水中被腐蚀,其负极反应为O2 +2H2O + 4e-=4OH-
C.可用被保护金属与直流电源负极相接的方法来减慢腐蚀速率
D.电解法精炼铜时,阳极材料应用粗铜
【答案】B
【解析】
A、铁比锡活沷,镀锡的铁片镀层破损后,腐蚀速率加快,A正确;
B、Fe在食盐水中被腐蚀,其负极反应为:Fe―2e-=Fe2+,B错误;
C、可用被保护金属与直流电源负极相接的方法来减慢腐蚀速率,即外加电流的阴极保护法,C正确;
D、电解法精炼铜时,阳极材料应用粗铜,阳极粗铜溶解,D正确;
答案选B。

【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(III)的处理工艺流程如下:

已知:①硫酸浸取液中的金属离子主要是Cr3+,其次是Fe2+、Al3+、Ca2+和Mg2+。②Cr2O72-+H2O![]() 2CrO42-+2H+。③常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
2CrO42-+2H+。③常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe2+ | Mg2+ | Al3+ | Cr3+ |
沉淀完全时的pH | 3.2 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
(1) 实验室用18.4mol/L的浓硫酸配制480mL2mol/L的硫酸,需量取浓硫酸_____mL;配制时除量筒、烧杯和玻璃棒外,还需用到的玻璃仪器有______________。
(2) H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:__________。
(3过滤II操作得到的滤渣主要为______(填化学式),滤液II中含有的离子主要有__。
(4) 钠离子交换树脂的反应原理为:Mn++nNaR=MRn+nNa+,则利用钠离子交换树脂可除去滤液II中的金属阳离子有_______________。
(5) 写出上述流程中用SO2进行还原时发生反应的离子方程式__________。
【题目】下列有关实验的选项正确的是
|
|
|
|
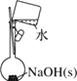
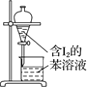
A.配制 0.10 mol·L-1NaOH溶液 | B.苯萃取碘水中I2,分出水层后的操作 | C.除去CO中的CO2 | D.记录滴定终点读数为12.20mL |
A. A B. B C. C D. D
【题目】在2 L密闭容器中进行反应:aX(s)+bY(g)![]() cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
物质 时间 | X | Y | P | Q |
起始/mol | 0.5 | 1.0 | 1.5 | |
2min末/mol | 0.7 | 2.7 | 0.8 | |
3min末/mol | 2.7 |
已知2 min内v(Q)=0.075 mol·L-1·min-1,v(P)∶v(Y)=2∶5。
(1)试确定以下物质的相关量:起始时n(Y)=______,2min末时n(Q)=______。
(2)上述反应的化学方程式为_________
(3)用Y表示2 min内的反应速率为______。2min末,Q在混合气体的体积分数为_____
(4)在保持温度和容积不变的情况下,下列关于上述反应的叙述不正确的是_____
a.2 min内用X表示的反应速率为0.05mol·L-1·min-1
b.向容器内充入稀有气体Ar(不参与反应),会导致体系压强增大,反应速率加快
c.随着反应的进行,混合气体的平均相对分子质量不再改变即说明反应已经达到平衡
d.随着反应的进行,混合气体的密度不再改变即说明反应已经达到平衡
e.随着反应的进行,混合气体的压强不再改变即说明反应已经达到平衡