题目内容
【题目】对于SO2和CO2的说法中正确的是( )
A. 都是直线形结构
B. 中心原子都采用SP杂化轨道
C. SO2为V形结构,CO2为直线形结构
D. S原子和C原子上都没有孤对电子
【答案】C
【解析】试题分析:A.SO2的价层电子对个数=2+![]() (6-2×2)=3,含有1个孤电子对,该分子为V形结构,CO2的价层电子对个数=2+
(6-2×2)=3,含有1个孤电子对,该分子为V形结构,CO2的价层电子对个数=2+![]() (4-2×2)=2,该分子是直线形结构,故A错误;B.SO2的价层电子对个数是3,所以硫原子采取sP2杂化,CO2的价层电子对个数是2,所以碳原子采取sP杂化,故B错误;C.SO2的价层电子对个数=2+
(4-2×2)=2,该分子是直线形结构,故A错误;B.SO2的价层电子对个数是3,所以硫原子采取sP2杂化,CO2的价层电子对个数是2,所以碳原子采取sP杂化,故B错误;C.SO2的价层电子对个数=2+![]() (6-2×2)=3,该分子为V形结构,CO2的价层电子对个数=2+
(6-2×2)=3,该分子为V形结构,CO2的价层电子对个数=2+![]() (4-2×2)=2,该分子是直线形结构,故C正确;D.SO2的孤电子对个数=
(4-2×2)=2,该分子是直线形结构,故C正确;D.SO2的孤电子对个数=![]() (6-2×2)=1,CO2的孤电子对个数=
(6-2×2)=1,CO2的孤电子对个数=![]() (4-2×2)=0,所以二氧化硫有1对孤对电子,二氧化碳没有孤对电子,故D错误。
(4-2×2)=0,所以二氧化硫有1对孤对电子,二氧化碳没有孤对电子,故D错误。

练习册系列答案
相关题目
【题目】符合右图的反应是
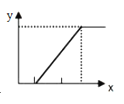
x轴 | y轴 | ||
A | 向氯化铝溶液中加入氢氧化钠溶液 | 氢氧化钠的物质的量 | 生成沉淀的质量 |
B | 向碳酸钠溶液中加入稀盐酸 | 盐酸的体积 | 产生气体的体积 |
C | 向溴化亚铁溶液中通入氯气 | 氯气的体积 | 生成Br2的物质的量 |
D | 向氢氧化钙溶液中通入二氧化碳 | 二氧化碳的体积 | 生成碳酸氢钙的质量 |