题目内容
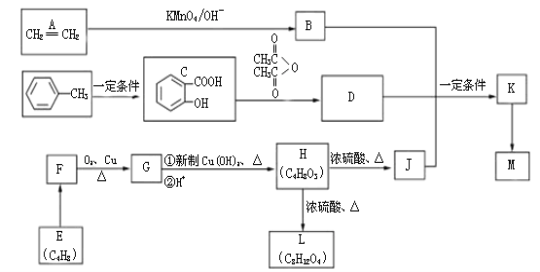
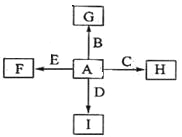
【题目】下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。
已知:
①反应![]() 能放出大量的热,该反应曾应用于铁轨的焊接;
能放出大量的热,该反应曾应用于铁轨的焊接;
②I是一种常见的温室气体,它和E可以发生反应:![]() ,F中E元素的质量分数为60%。
,F中E元素的质量分数为60%。
回答问题:
(1)①中反应的化学方程式为 ;
(2)化合物I的电子式为 ;
(3)C与过量NaOH溶液反应的离子方程式为 ,反应后溶于与过量化合物I反应的离子方程式为 ;
(4)E在I中燃烧观察到的现象是 。
【答案】(1)2Al+Fe2O3![]() Al2O3+2Fe(2)
Al2O3+2Fe(2)![]() 。
。
(3)2Al+2OH-+2H2O=2AlO2-+3H2↑,AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-。
(4)镁条剧烈燃烧,生成白色固体,同时集气瓶内壁上有黑色固体附着。
【解析】
试题分析:根据题给信息和转化关系推断,根据信息①推断,C为铝,B为铁,H为氧化铝,G为氧化铁;根据信息②:二氧化碳是温室气体,所以I是二氧化碳;二氧化氮和E反应发反应生成F,F中E元素的质量分数为60%,则E为镁,F为氧化镁,D为碳,A为氧气。
(1)①中反应的化学方程式为2Al+Fe2O3![]() Al2O3+2Fe。
Al2O3+2Fe。
(2)二氧化碳的电子式为![]() 。
。
(3)铝与过量NaOH溶液反应生成偏铝酸钠和氢气,离子方程式为2Al + 2OH- + 2H2O=2AlO2- + 3H2↑,偏铝酸钠溶液与过量二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,离子方程式为AlO2- + CO2 + 2H2O=Al(OH)3↓+ HCO3- 。
(4)镁在二氧化碳中燃烧观察到的现象是镁条剧烈燃烧,生成白色固体,同时集气瓶内壁上有黑色固体附着。

练习册系列答案
相关题目