题目内容
【题目】一个体重50kg的健康人体内含铁元素2g,这2g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。请回答下列问题:
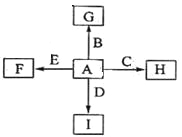
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____________。
A .Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中__________是氧化剂,说明维生素C具有 性。
(3)在人体中进行Fe2+![]() Fe3+的转化时,①反应中的Fe2+发生 反应,②反应中的Fe3+被_______________。
Fe3+的转化时,①反应中的Fe2+发生 反应,②反应中的Fe3+被_______________。
(4)市场上出售的某种麦片中含有微量的颗粒细小的还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为___________________________,离子方程式为_________________________。
(5)己知下列反应:
①H2O2+2Fe3+=2Fe2++O2↑+2H+②2Fe2++H2O2+2H+=2Fe3++2H2O
反应①中生成1 molO2转移电子的物质的量为__________,反应①、②的总反应方程式为______________________,
在该反应中Fe3+的作用为________________。
(6)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中, HNO3表现了___________性和_____________ 性,毎有1 molFe参加反应转移电子______________mol。
【答案】(1)B;(2)Fe3+;还原;(3)氧化;还原
(4)Fe+2HCl==FeCl2+H2↑Fe+2H+==Fe2++H2↑
(5)2mol;2H2O2==2H2O+O2↑;催化剂;(6)酸;氧化;3
【解析】
试题分析:(1)元素具有变价时,最低价只有还原性,最高价只有氧化性,中间价态,具有两性;A.Fe只有还原性B.Fe2+既有氧化性,又有还原性;C.Fe3+只有氧化性;(2)Fe3+转化为Fe2+,Fe3+做氧化剂;维生素C具有还原性;(3)Fe2+→Fe3+发生氧化反应;Fe3+→Fe2+,Fe3+被还原;(4)胃液主要成分为盐酸,铁与盐酸反应:Fe+2HCl===FeCl2+H2↑;Fe+2H+===Fe2++H2↑;
(5)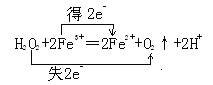 生成1molO2转移电子的物质的量2mol;①②两式相加,得2H2O2==2H2O+O2↑;Fe3+反应前后质量和性质保持不变,起作用催化剂;(6)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,硝酸被还原,表现氧化性,生成硝酸盐,表现酸性;毎有1 molFe参加反应转移电子3mol。
生成1molO2转移电子的物质的量2mol;①②两式相加,得2H2O2==2H2O+O2↑;Fe3+反应前后质量和性质保持不变,起作用催化剂;(6)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,硝酸被还原,表现氧化性,生成硝酸盐,表现酸性;毎有1 molFe参加反应转移电子3mol。

【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl22H2O的流程如下:
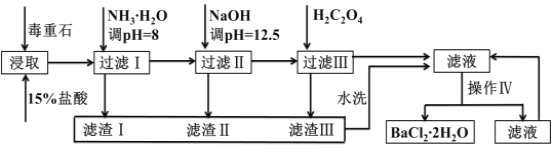
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀的pH | 11.9 | 9.1 | 1.9[ |
完全沉淀的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)= 1.6×10–7,Ksp(CaC2O4)= 2.3×10–9
(1)实验室用37%的盐酸配制1mol/L盐酸,下列仪器中,不需要使用的是_______ __
a.容量瓶 b.量筒 c.烧杯 d.滴定管
为了加快毒重石的酸浸速率,可以采取的措施有______________(至少两条)。
(2)加入氨水调节溶液pH=8的目的是___________________________。滤渣Ⅱ中含________(填化学式)。加入H2C2O4时应避免过量,原因是___ __ ____________。
(3)操作Ⅳ的步骤是:______ ______、过滤。
(4)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42—+2H+=Cr2O72—+H2O ;Ba2++CrO42— =BaCrO4↓
步骤Ⅰ:移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL。
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL。
通过计算,氯化钡溶液浓度为___________mol·L-1(用含字母的式子表示)。