题目内容
【题目】硫酸铜可用于消毒、制杀虫剂、镀铜等。实验小组制取CuSO4·5H2O晶体并进行热分解的探究。请回答以下问题:
探究Ⅰ:制取CuSO4·5H2O晶体
小组同学设计了如下两种方案:
甲:将铜片加入足量浓硫酸中并加热
乙:将铜片加入稀硫酸,控温40~50℃,滴加双氧水
(1)方案甲发生反应的化学方程式为____________,反应结束后有大量白色固体析出。简述从中提取CuSO4·5H2O晶体的方法:倒出剩余液体,____________。
(2)方案乙发生反应:Cu+H2SO4+H2O2=CuSO4+2H2O,该实验控温40~50℃的原因是________;与方案甲相比,方案乙的主要优点有_________、___________。(写出2种)
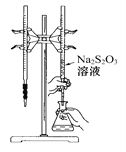
探究Ⅱ:用以下装置(加热装置省略)探究CuSO4·5H2O晶体热分解产物

已知:CuSO4·5H2O脱水后升高温度,会继续分解成CuO和气体产物,气体产物可能含有SO3、SO2、O2中的1~3种。
(3)称5.00gCuSO4·5H2O于A中加热,当观察到A中出现_____________,可初步判断晶体已完全脱水并发生分解。加热一段时间后,A中固体质量为3.00g,则此时A中固体的成分为___________。
(4)装置B中迅速生成白色沉淀,说明分解产物中有__________,C装置的作用是____________。
(5)理论上E中应收集到VmL气体,事实上体积偏少,可能的原因是______________。(不考虑泄漏等仅器与操作原因)。
【答案】 .Cu+2H2SO4(浓) ![]() SO2↑+CuSO4+2H2O 加入适量水,蒸发浓缩,冷却结晶 温度较低,反应速率慢;温度太高,H2O2分解,损耗大 原料利用率高 不产生污染等合理答案 固体变为黑色 CuSO4 和 CuO SO3 检验有SO2生成 在C装置中部分O2参与了氧化还原反应
SO2↑+CuSO4+2H2O 加入适量水,蒸发浓缩,冷却结晶 温度较低,反应速率慢;温度太高,H2O2分解,损耗大 原料利用率高 不产生污染等合理答案 固体变为黑色 CuSO4 和 CuO SO3 检验有SO2生成 在C装置中部分O2参与了氧化还原反应
【解析】本题主要考查对于“制取CuSO4·5H2O晶体并进行热分解”的探究实验的评价。
(1)方案甲发生反应的化学方程式为Cu+2H2SO4(浓) ![]() SO2↑+CuSO4+2H2O,反应结束后有大量白色固体析出。从中提取CuSO4·5H2O晶体的方法:倒出剩余液体,加入适量水,蒸发浓缩,冷却结晶。
SO2↑+CuSO4+2H2O,反应结束后有大量白色固体析出。从中提取CuSO4·5H2O晶体的方法:倒出剩余液体,加入适量水,蒸发浓缩,冷却结晶。
(2)方案乙发生反应:Cu+H2SO4+H2O2=CuSO4+2H2O,该实验控温40~50℃的原因是温度较低,反应速率慢;温度太高,H2O2分解,损耗大 ;与方案甲相比,方案乙的主要优点有原料利用率高、不产生污染等合理答案。
探究Ⅱ:
(3)若5.00gCuSO4·5H2O完全成为CuO,则质量为1.6g。加热一段时间后,A中固体质量为3.00g>1.6g,则此时A中固体的成分为CuSO4 和 CuO。
(4)装置B中迅速生成白色沉淀,说明分解产物中有SO3,C装置的作用是检验有SO2生成。
(5)理论上E中应收集到VmL气体,事实上体积偏少,可能的原因是在C装置中部分O2参与了氧化还原反应。

【题目】合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
温 度(℃) | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①由上表数据可知该反应的ΔH_____ 0(填填“>”、“=”或“<”)。
②下列措施能用勒夏特列原理解释是_____(填序号)。
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500°C左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol NH3溶于水后再与含有0.2mol H2SO4的稀溶液完全反应放热Q kJ,请你用热化学方程式表示其反应式:___________________________________。
(3)常温时,将a mol氨气溶于水后,再通入b mol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl﹣),则一水合氨的电离平衡常数Kb=_____(用ab表示)。
(4)原料气H2可通过反应 CH4(g)+H2O (g)![]() CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的![]() 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
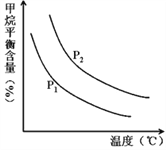
①图中,两条曲线表示压强的关系是:P1_____P2(填“>”、“=”或“<”)。
②其它条件一定,升高温度,氢气的产率会______(填“增大”,“减小”减小,“不变”不变)。
(5)原料气H2还可通过反应CO(g)+H2O(g)![]() CO2(g)+H2(g)获取。
CO2(g)+H2(g)获取。
①T℃时,向容积固定为5 L的容器中充入1mol H2O(g)和1mol CO, 反应达平衡后,测得CO的浓度0.08 mol/L,该温度下反应的平衡常数K值为_____。
②保持温度仍为T℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是_____(填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6