题目内容
18.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑩十种元素在周期表中的位置:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ⑩ | ||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑤ | ⑨ |
(1)十种元素中化学性质最不活泼的是He(填元素符号 ).
(2)在②、③、④三种元素的氧化物对应的水化物中,碱性最强 的是NaOH(填化学式 ),其中含有化学键的类型有离子键、共价键.
(3)元素①、②、⑤原子半径由大到小的顺序为K>Na>H(填元素符号 ).
(4)元素⑦、⑧、⑨氢化物的稳定性由强到弱的顺序为HF>HCl>HBr(填化学式 ).
(5)十种元素中有一种元素的氢化物水溶液呈碱性,该氢化物的电子式为
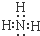 .
.(6)十种元素中Al(填元素符号 )的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑.
分析 由元素在周期表中的位置可知,①为H、②为Na、③为Mg、④为Al、⑤为K、⑥为C、⑦为F、⑧为Cl、⑨为Br、⑩为He.
(1)稀有气体原子最外层为稳定结构,化学性质最不活泼;
(2)金属性越强,最高价氧化物对应水化物的碱性越强;
(3)同主族自上而下原子半径增大;
(4)同主族自上而下非金属性减弱,非金属性越强,氢化物越稳定;
(5)上述元素的氢化物水溶液呈碱性为NH3;
(6)Al单质能与盐酸、氢氧化钠反应反应,与氢氧化钠溶液反应生成偏铝酸钠与氢气.
解答 解:由元素在周期表中的位置可知,①为H、②为Na、③为Mg、④为Al、⑤为K、⑥为C、⑦为F、⑧为Cl、⑨为Br、⑩为He.
(1)稀有气体He原子最外层为稳定结构,化学性质最不活泼,故答案为:He;
(2)金属性Na>Mg>Al,金属性越强,最高价氧化物对应水化物的碱性越强,故NaOH的碱性最强,含有离子键、共价键,故答案为:NaOH;离子键、共价键;
(3)同主族自上而下原子半径增大,故原子半径:K>Na>H,故答案为:K>Na>H;
(4)同主族自上而下非金属性减弱,非金属性越强,氢化物越稳定,故氢化物稳定性:HF>HCl>HBr,故答案为:HF>HCl>HBr;
(5)上述元素的氢化物水溶液呈碱性为NH3,电子式为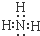 ,故答案为:
,故答案为: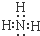 ;
;
(6)上述元素中Al单质能与盐酸、氢氧化钠反应反应,与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:Al;2Al+2OH-+2H2O═2AlO2-+3H2↑.
点评 本题考查元素周期律与元素周期表,难度不大,侧重对基础知识的巩固,需要学生熟练掌握基础知识,注意对元素周期律的理解应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料.下列实验事实与硝酸性质不相对应的一组是( )
| A. | 浓硝酸使紫色石蕊试液先变红后褪色--酸性和强氧化性 | |
| B. | 不能用稀硝酸与锌反应制氢气--强氧化性 | |
| C. | 要用棕色瓶盛装浓硝酸--不稳定性 | |
| D. | 稀硝酸能使滴有酚酞的氢氧化钠溶液红色褪去--强氧化性 |
9.由2-氯丙烷为主要原料制取1,2-丙二醇,经过的反应为( )
| A. | 加成-消去-取代 | B. | 消去-加成-取代 | C. | 取代-消去-加成 | D. | 取代-加成-消去 |
6.下列关于原子的几种描述中,不正确的是( )
| A. | 18O与19F具有相同的中子数 | |
| B. | 16O与17O具有相同的电子数,互为同位素 | |
| C. | 15N与14N具有相同的质子数,是同种核素 | |
| D. | 12C与13C具有不同的质量数,属于同种元素 |
13.下列叙述中能肯定说明金属A比金属B的活泼的是( )
| A. | A原子电子层数比B原子的电子层数多 | |
| B. | 常温时,A能从稀酸中置换出氢,而B不能 | |
| C. | A原子最外层电子数比B原子的最外层电子数少 | |
| D. | 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 |
3.下列各组离子在指定溶液中肯定大能量共存的是( )
| A. | 石蕊溶液呈蓝色的溶液:K+、Na+、NO3-、Cl- | |
| B. | 无色透明溶液中:MnO4-、K+、Na+、NO3- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、NH4+、NO3- | |
| D. | 酸性溶液中:Al3+、Na+、SO42-、HCO3- |
10.有关电解质与非电解质的陈述,合理的是( )
| A. | 在水溶液中能导电的化合物都是电解质 | |
| B. | 在熔融状态下不导电的化合物都是非电解质 | |
| C. | 氨水为混合物,不属于电解质 | |
| D. | 硫酸溶于水能导电,所以浓硫酸为电解质 |
7.F、Cl和Br都是 VIIA族元素,关于这三种元素原子的说法正确的是( )
| A. | 原子半径:F>Cl>Br | B. | 最外层电子数都相同 | ||
| C. | 核外电子层数都相同 | D. | 最外层电子数依次增多 |
3.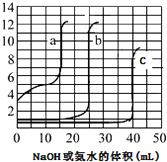 取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol•L-1的NaOH溶液或0.10mol•L-1 的稀氨水滴定得如图.下列说法正确的是( )
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol•L-1的NaOH溶液或0.10mol•L-1 的稀氨水滴定得如图.下列说法正确的是( )
 取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol•L-1的NaOH溶液或0.10mol•L-1 的稀氨水滴定得如图.下列说法正确的是( )
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol•L-1的NaOH溶液或0.10mol•L-1 的稀氨水滴定得如图.下列说法正确的是( )| A. | 由图可知曲线c为NaOH滴定硫酸 | |
| B. | 由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度 | |
| C. | 曲线b、c的滴定实验可用酚酞做指示剂 | |
| D. | 由图可知滴定前醋酸电离度约为1.67% |