题目内容
9.由2-氯丙烷为主要原料制取1,2-丙二醇,经过的反应为( )| A. | 加成-消去-取代 | B. | 消去-加成-取代 | C. | 取代-消去-加成 | D. | 取代-加成-消去 |
分析 2-氯丙烷为主要原料制取1,2-丙二醇CH3CH(OH)CH2OH,-Cl变化为两个-OH,应先消去生成C=C,再加成引入两个卤素原子,最后水解即可,以此来解答.
解答 解:2-氯丙烷为主要原料制取1,2-丙二醇CH3CH(OH)CH2OH,
①先发生氯代烃的消去反应生成C=C,
②再发生丙烯的加成反应引入两个卤素原子,
③最后发生卤代烃的水解反应(属于取代反应)生成CH3CH(OH)CH2OH,故选B.
点评 本题考查有机物的合成,注意官能团的变化,结合卤代烃、烯烃的性质即可解答,题目难度不大.

练习册系列答案
相关题目
19.试管中盛有白色晶体,检验它是否是铵盐的方法中不可行的是( )
| A. | 加热,将湿润的红色石蕊试纸放在管口 | |
| B. | 加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口 | |
| C. | 加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在试管口 | |
| D. | 加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在管口 |
20.密闭容器中可逆反应H2(g)+I2(g)?2HI(g)达到平衡的标志是( )
| A. | H2、I2、HI的浓度相等 | B. | H2、I2、HI的浓度保持不变 | ||
| C. | 混合气体的密度保持不变 | D. | 混合气体的压强不再改变 |
17.下列各组物质中,前者为附着在容器内壁的污物,后者能除去前者的药品是( )
①银镜-硝酸
②油脂-热Na2CO3溶液
③水垢-醋酸
④硫黄-CS2
⑤苯酚-酒精.
①银镜-硝酸
②油脂-热Na2CO3溶液
③水垢-醋酸
④硫黄-CS2
⑤苯酚-酒精.
| A. | 只有①③⑤ | B. | 只有①④⑤ | C. | 只有②③⑤ | D. | 全部 |
1.常用特定图案来表示危险化学品的类别.下列组合中图案与化学品性质相符的是( )
| A. |  H2 | B. |  浓盐酸 | C. |  浓硫酸 | D. |  CO2 |
18.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.
下表列出了①~⑩十种元素在周期表中的位置:
请回答下列问题:
(1)十种元素中化学性质最不活泼的是He(填元素符号 ).
(2)在②、③、④三种元素的氧化物对应的水化物中,碱性最强 的是NaOH(填化学式 ),其中含有化学键的类型有离子键、共价键.
(3)元素①、②、⑤原子半径由大到小的顺序为K>Na>H(填元素符号 ).
(4)元素⑦、⑧、⑨氢化物的稳定性由强到弱的顺序为HF>HCl>HBr(填化学式 ).
(5)十种元素中有一种元素的氢化物水溶液呈碱性,该氢化物的电子式为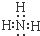 .
.
(6)十种元素中Al(填元素符号 )的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑.
下表列出了①~⑩十种元素在周期表中的位置:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ⑩ | ||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑤ | ⑨ |
(1)十种元素中化学性质最不活泼的是He(填元素符号 ).
(2)在②、③、④三种元素的氧化物对应的水化物中,碱性最强 的是NaOH(填化学式 ),其中含有化学键的类型有离子键、共价键.
(3)元素①、②、⑤原子半径由大到小的顺序为K>Na>H(填元素符号 ).
(4)元素⑦、⑧、⑨氢化物的稳定性由强到弱的顺序为HF>HCl>HBr(填化学式 ).
(5)十种元素中有一种元素的氢化物水溶液呈碱性,该氢化物的电子式为
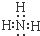 .
.(6)十种元素中Al(填元素符号 )的单质既可以和盐酸又可以和氢氧化钠溶液反应,其单质与氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑.