题目内容
8.孔雀石主要含Cu2(OH)2CO3,还含少量FeO、SiO2.以孔雀石为原料可制备CuSO4•5H2O步骤如下: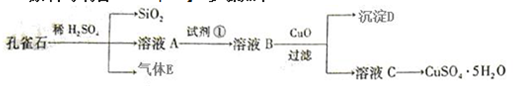
(1).写出孔雀石与稀硫酸反应的化学方程式:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2,
为了提高原料浸出速率,可采取的措施有增加硫酸浓度、将原料粉碎提高反应温度,加催化剂等(写出两条).
(2).溶液A的金属离子有Cu2+、Fe2+.实验步骤中试剂①最佳选c (填代号).
a.KMnO4 b.Cl2 c.H2O2 d.HNO3
(3)溶液B中加入CuO作用是调pH值,(或减少c(H+),)使Fe3+沉淀完全.
(4)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10-3mol/L,必需将溶液pH调节至2.
(5)由溶液C获得CuSO4•5H2O晶体,需要经蒸发浓缩(或加热蒸发、蒸发溶液)、冷却结晶和过滤.
(6)可用KMnO4标准溶液测定溶液A中Fe2+的浓度,量取A溶液20.00ml,用0.010mol/L酸性KMnO4标准溶液滴定,消耗KMnO410.00ml,A溶液中Fe2+的物质的量浓度0.025mol/L.
(反应原理:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O)
分析 孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,向孔雀石中加入足量稀硫酸,发生的反应有Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,Fe+H2SO4=FeSO4+H2↑,硅和稀硫酸不反应,溶液A只含Cu2+、Fe2+两种金属离子,然后过滤得到的滤渣中含有Si的氧化物,溶液A中含有含有铁盐和亚铁盐及硫酸铜,气体E为CO2、H2,向溶液A中加入试剂①得到溶液B,试剂①是一种氧化剂,将Fe2+转化为Fe3+且不能引进杂质,可选取双氧水,向溶液B中加入试剂②经过操作Ⅰ得到溶液C和红褐色沉淀D,则操作Ⅰ为过滤,D为Fe(OH)3,以及过量的试剂,溶液C为硫酸铜溶液,所以为试剂②为CuO或Cu(OH)2或CaCO3 或Cu2(OH)2CO3,据此答题.
(1)碱式碳酸铜为碱式盐能与稀硫酸反应,依据影响化学反应速率的因素分析判断;
(2)双氧水是一种绿色试剂,将Fe2+氧化为Fe3+,但无明显现象;
(3)在溶液B中加CuO调节溶液的pH使Fe3+完全沉淀,且不引入新的杂质;
(4)依据溶度积常数计算氢氧根离子浓度,结合离子积常数计算氢离子浓度得到溶液PH;
(5)溶液中得到溶质的方法是经蒸发浓缩(或加热蒸发、蒸发溶液),冷却结晶、过滤,得到溶质;
(6)Fe2+溶液与KMnO4溶液发生氧化还原反应,反应中MnO4-被还原为Mn2+,最小公倍数为5,所以KMnO4前系数为1,Fe2+前系数为5,结合原子守恒和电荷守恒配平写出离子方程式,结合定量关系计算亚铁离子浓度.
解答 解:孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,向孔雀石中加入足量稀硫酸,发生的反应有Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,Fe+H2SO4=FeSO4+H2↑,硅和稀硫酸不反应,溶液A只含Cu2+、Fe2+两种金属离子,然后过滤得到的滤渣中含有Si的氧化物,溶液A中含有含有铁盐和亚铁盐及硫酸铜,气体E为CO2、H2,向溶液A中加入试剂①得到溶液B,试剂①是一种氧化剂,将Fe2+转化为Fe3+且不能引进杂质,可选取双氧水,向溶液B中加入试剂②经过操作Ⅰ得到溶液C和红褐色沉淀D,则操作Ⅰ为过滤,D为Fe(OH)3,以及过量的试剂,溶液C为硫酸铜溶液,所以为试剂②为CuO或Cu(OH)2或CaCO3 或Cu2(OH)2CO3,
(1)碱式碳酸铜为碱式盐能与稀硫酸反应:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,生成硫酸铜、水和二氧化碳,为了提高原料浸出速率,可采取的措施有增加硫酸浓度、将原料粉碎、提高反应温度,加催化剂等,
故答案为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;增加硫酸浓度、将原料粉碎、提高反应温度,加催化剂等;
(2)Fe2+具有还原性,可被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,与KSCN不反应,加入氢氧化钠溶液可生成氢氧化铁、氢氧化铜沉淀而不能检验Fe2+,双氧水,双氧水是一种绿色试剂,将Fe2+氧化为Fe3+,但无明显现象,只有b正确,
故答案为:c;
(3)在溶液B中加CuO调节溶液的pH使Fe3+完全沉淀,且不引入新的杂质,
故答案为:调pH值,(或减少c(H+),)使Fe3+沉淀完全;
(4)常温下Fe(OH)3的Ksp=1×10-39,使溶液中c(Fe3+)=1×10-3mol/L,则c(OH-)=$\root{3}{\frac{1×10{\;}^{-39}}{1×10{\;}^{-3}}}$mol/L=1×10-12mol/L,所以溶液中c(H+)=1×10-2mol/L,则pH=2,
故答案为:2;
(5)CuSO4•5H2O晶体,在高温时易失去水,所以从溶液中获得CuSO4•5H2O晶体,需要经蒸发浓缩(或加热蒸发、蒸发溶液),冷却结晶、过滤,
故答案为:蒸发浓缩(或加热蒸发、蒸发溶液)、冷却结晶;
(6)Fe2+溶液与KMnO4溶液发生氧化还原反应,反应中MnO4-被还原为Mn2+,最小公倍数为5,所以KMnO4前系数为1,Fe2+前系数为5,反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,根据离子方程可知MnO4-~5Fe2+,用去 KMnO4的物质的量为10.00mL×0.010mol/L=1.0×10-4mol,所以A溶液中Fe2+浓度为$\frac{1.0×10{\;}^{-4}mol×5}{0.02L}$=0.025mol/L,
故答案为:0.025.
点评 本题考查以孔雀石为主要原料制备CuSO4•5H2O及纳米材料,为高频考点和常见题型,侧重于学生的分析、实验和计算能力得到考查,注意把握实验的原理以及物质的性质,为解答该类题目的关键,注意掌握实验基本操作和流程分析,题目难度中等.

| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
①CS2为V形的极性分子
②ClO3-的空间构型为平面三角形
③SF6中有6对完全相同的成键电子对
④SiF4和SO32-的中心原子均为sp3杂化.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
(1)精炼铜时,阴极材料是纯铜,阴极的电极反应式是Cu2++2e-=Cu,
(2)氯碱工业电解饱和食盐水的总反应方程式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
(3)MnO2可作超级电容器材料.用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是Mn2++2H2O-2e-=MnO2+4H+
(4)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-离子.电池工作时正极反应式为O2+4e-=2O2-.
若以该电池为电源,用石墨做电极电解100mL含有如下离子的液.
| 离子 | Cu2+ | H+ | Cl- | SO$\stackrel{2-}{4}$ |
| c/(mol•L-1) | 1 | 4 | 4 | 1 |
| A. | Cl2 | B. | NaOH | C. | H2O | D. | NaClO3 |
| A. | 气态氢化物的稳定性:Y>X>W | |
| B. | 四种元素的原子中W原子半径最大 | |
| C. | 四种元素中最高价氧化物的水化物酸性Y最强 | |
| D. | 化合物XY2与ZY2分子中的化学键类型相同 |
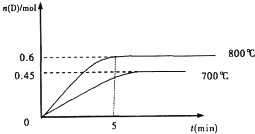 在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.试回答下列问题:
在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图.试回答下列问题: