题目内容
6.将100mL 3mol•L-1的NaOH溶液与100mL 3mol•L-1的AlCl3溶液按下列两种方法混合:(1)将NaOH溶液逐滴入AlCl3溶液中;
(2)将AlCl3溶液逐滴滴入NaOH溶液中,对上述实验所得结论正确的是( )
| A. | 现象相同,沉淀量相等 | B. | 现象相同,沉淀量不等 | ||
| C. | 现象不同,沉淀量相等 | D. | 现象不同,沉淀量不等 |
分析 将NaOH溶液逐滴加入AlCl3溶液中,发生:Al3++3OH-═Al(OH)3↓,将AlCl3溶液逐滴加入NaOH溶液中,分别发生:Al3++4OH-=AlO2-+2H2O,Al3++3AlO2-+6H2O=4Al(OH)3↓,以此进行判断.
解答 解:100mL 3mol•L-1NaOH溶液中n(NaOH)=0.3mol,100mL 3mol•L-1的AlCl3溶液中n(AlCl3)=0.3mol,则
①将NaOH溶液逐滴加入AlCl3溶液中,发生:Al3++3OH-═Al(OH)3↓,现象为观察到白色沉淀,生成沉淀为0.1mol,②将AlCl3溶液逐滴加入NaOH溶液中,分别发生:Al3++4OH-=AlO2-+2H2O,生成$\frac{0.3}{4}$molAlO2-,Al3++3AlO2-+6H2O=4Al(OH)3↓,铝离子过量,生成沉淀为0.1mol,先没有沉淀后出现沉淀,
所以二者现象不同,但沉淀质量相等.
故选C.
点评 本题考查的化合物的性质,题目难度不大,学习中注意相关基础知识的积累,特别是铝三角知识,为中学元素化合物中的重要内容.

| A. | 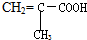 | B. | 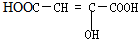 | C. | HCOOCH=CHCOOH | D. | CH2=C-COOCH3 |
| A. | 变大 | B. | 变小 | C. | 不变 | D. | 无法确定 |
| A. | 原子半径:Te>Cl>S | B. | 热稳定性:H2Te>H2S>PH3 | ||
| C. | 还原性:Cl->S2->Te2- | D. | 酸性:HClO4>H2SO4>H2TeO4 |
甲、乙两个小组利用酸性KMnO4与H2C2O4溶液反应,设计实验探究影响反应速率的因素(2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2+8H2O)
甲组:利用如图装置,通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小.(实验中所用KMnO4溶液均已加入H2SO4)

序号 | A溶液 | B溶液 |
① | 2ml 0.2mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液 |
② | 2ml 0.1mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液 |
③ | 2ml 0.2mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液和少量MnSO4 |
(1)该实验的目的是探究________________对化学反应速率的影响.
(2)分液漏斗中A溶液应该_____________加入(填“一次性”或“逐滴滴加”)
(3)实验结束后,读数前为了使两个量气管的压强相等,避免产生压强差,影响测定结果,需要进行的操作是____________________.
乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率为了探究KMnO4与H2C2O4浓度对反应速率的影响,某同学在室温下完成以下实验
实验编号 | 1 | 2 | 3 | 4 |
水/ml | 10 | 5 | 0 | X |
0.5mol/L H2C2O4/ml | 5 | 10 | 10 | 5 |
0.2mol/L KMnO4/ml | 5 | 5 | 10 | 10 |
时间/s | 40 | 20 | 10 | ﹣﹣﹣ |
(4)X=____________
A.5 B.10 C.15 D.20
4号实验中始终没有观察到溶液褪色,你认为可能的原因是____________
(已知Ksp[Fe(OH)3]=3.8×10-38; Ksp[Cu(OH)2]=2×10-20;Ksp(ZnS)=1.6×10-24)
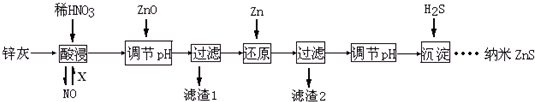
下列说法不正确的是( )
| A. | 酸浸时FeO与稀HNO3反应的离子方程式为3FeO+10H++NO${\;}_{3}^{-}$═3Fe3++NO↑+5H2O | |
| B. | 将酸浸的尾气循环利用,加入的X气体可以是O2 | |
| C. | 滤渣2中的成分和Zn和Fe | |
| D. | 当溶液中Zn2+浓度为小于1.0×10-5mol•L-1时,则可认为其沉淀完全.若要使Zn2+沉淀完全,溶液中S2-浓度应大于1.6×10-19mol•L-1 |
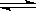 A2(g)+B2(g)达到平衡状态的标志是( )
A2(g)+B2(g)达到平衡状态的标志是( ) nmolA2的同时消耗n molAB
nmolA2的同时消耗n molAB