题目内容
1.已知16S和52Te位于同一主族,下列关系正确的是( )| A. | 原子半径:Te>Cl>S | B. | 热稳定性:H2Te>H2S>PH3 | ||
| C. | 还原性:Cl->S2->Te2- | D. | 酸性:HClO4>H2SO4>H2TeO4 |
分析 元素周期表中,同一周期元素从左到右,原子半径逐渐减小、非金属性逐渐增强,同主族自上而下,原子半径增大、元素的非金属性减弱,元素的非金属性越强,对应的氢化物越稳定,阴离子的还原性越弱,最高价氧化物对应的水化物的酸性越强,
A.同周期元素,原子半径随着原子序数增大而减小,同主族自上而下原子半径增大;
B.非金属的非金属性越强,其氢化物越稳定;
C.非金属的非金属性越强,其阴离子的还原性越弱;
D.非金属的非金属性越强,其最高价含氧酸的酸性越强.
解答 解:A.同周期元素从左到右,原子半径逐渐减小,同主族元素从上到下,原子半径逐渐增大,则应有Te>S>Cl,故A错误;
B.非金属性S>P>Te,元素的非金属性越强,对应的氢化物越稳定,故B错误;
C.非金属性Cl>S>Te,元素的非金属性越强,对应的阴离子的还原性越弱,则还原性Te2->S2->Cl-,故C错误;
D.非金属性Cl>S>Te,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性HClO4>H2SO4>H2TeO4,故D正确,
故选D.
点评 本题考查元素周期律知识,侧重于学生的分析应用能力的考查,注意把握同主族、同周期元素化合物的性质的相似性与递变性,难度不大.

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案| A. | 过氧化钠 | B. | 二氧化硫 | C. | 双氧水 | D. | 活性炭 |
| A. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 | |
| B. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 | |
| C. | 煤油可由石油分馏获得,可用作燃料和保存少量金属钠 | |
| D. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
(1)将NaOH溶液逐滴入AlCl3溶液中;
(2)将AlCl3溶液逐滴滴入NaOH溶液中,对上述实验所得结论正确的是( )
| A. | 现象相同,沉淀量相等 | B. | 现象相同,沉淀量不等 | ||
| C. | 现象不同,沉淀量相等 | D. | 现象不同,沉淀量不等 |
把温度为20℃,浓度为1.0mol·L-1的H2SO4和2.2mol·L-1的碱溶液各50ml混合(溶液密度均为1g·ml-1,比热容为4.184kJ·K-1·kg-1),轻轻搅动。测得酸碱混合液的温度变化数据如下:
反应物 | 起始温度t1℃ | 终止温度t2℃ |
H2SO4+NaOH | 20 | 33.6 |
H2SO4+NH3·H2O | 20 | 32.6 |
则反应NH3·H2O=NH4++OH-的焓变约为( )(单位:kJ·mol-1)
A.2.1 B.4.2 C.52.7 D. 缺少数据无法计算
Ⅰ、高铁酸钠(Na2FeO4)是一种新型净水剂,工业上制备高铁酸钠的方法之一的反应原理为:Fe(OH)3+NaClO+NaOH→Na2FeO4+X+H2O,则X的化学式NaCl,反应中被氧化的物质是Fe(OH)3(写化学式).
Ⅱ、铁红颜料跟某些油料混合,可以制成防锈油漆.工业制硫酸产生的硫酸渣中主要含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
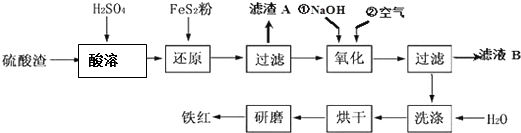
已知:①
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4) 3+3H2O;“滤渣A”主要成份的化学式为SiO2.
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,写出该反应的离子方程式:FeS2+14 Fe3++8 H2O=15Fe2++2 SO42-+16 H+.
(3)为了确保铁红的质量和纯度,氧化过程中加NaOH调节溶液的pH的范围是3.2~3.8;如果加NaOH调节溶液的pH=a,则滤液B中的c(Fe3+)=4×10(4-3a)(25℃时,Ksp[Fe(OH)3]=4×10-38)
(4)滤液B中可以回收的物质有Na2SO4、Al2(SO4)3、MgSO4.
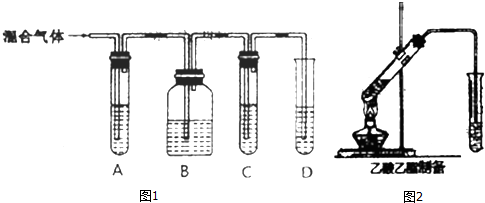
 CH3COOCH2CH3+H2O,该反应类型为酯化反应(取代反应).
CH3COOCH2CH3+H2O,该反应类型为酯化反应(取代反应). 2SO3(g)△H<0
2SO3(g)△H<0 浓度由6mol/L下降为2mol/L,那么,用O2浓度变化来表示的反应速率为 .
浓度由6mol/L下降为2mol/L,那么,用O2浓度变化来表示的反应速率为 .