题目内容
【题目】X、Y、Z、W均为短周期主族元素,它们在周期表中的相对位置如图所示,下列说法中不正确的是( )
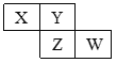
A. Y的价层电子排布式可能是ns2np4
B. 四种元素所形成的氢化物中,沸点最高的可能是Y的氢化物
C. Y、Z之间可形成离子化合物
D. X、Z、W的最高价氧化物所对应的水化物可能都是强酸
【答案】C
【解析】
X、Y、Z、W均为短周期主族元素,由它们在周期表中的相对位置可知,X、Y在第2周期,Z、W在第3周期,若X为碳元素、Y为氮元素,Z为磷元素、W为硫元素;若X为氮元素、Y为氧元素,Z为硫元素、W为氯元素,据此解答。
A、若X为氮元素、Y为氧元素,O的价层电子排布式可能是2s22p4,故A正确;
B、若X为氮元素、Y为氧元素,Z为硫元素、W为氯元素,四种元素所形成的氢化物依次为NH3、H2O、H2S、HCl,Y的氢化物为水,因水中含有氢键,所以四种元素所形成的氢化物中,Y的沸点最高,故B正确;
C、若Y为氮元素,Z为磷元素;若Y为氧元素,Z为硫元素,Y、Z均为非金属元素,Y、Z之间形成共价化合物,故C错误;
D、若X为氮元素、Y为氧元素,Z为硫元素、W为氯元素,X、Z、W的最高价氧化物所对应的水化物依次为HNO3、H2SO4、HClO4,均为强酸,故D正确。
故选C。

练习册系列答案
相关题目
【题目】用如图所示装置进行实验,下列对实验现象的解释不合理的是

选项 | ①试剂 | ①中现象 | 解释 |
A | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
B | Na2SiO3溶液 | 产生胶状沉淀 | 酸性: H2SO3 >H2SiO3 |
C | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
D | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成 白色BaSO3沉淀 |
A.AB.BC.CD.D