题目内容
某温度下,在一个2L的密闭容器中,加入4molA和2molB进行如下反应:
3A(g)+2B(g) 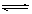 4C(s) +2D(g)反应一段时间后达到平衡,测得生成1.6molC。则下列说法正确的是
4C(s) +2D(g)反应一段时间后达到平衡,测得生成1.6molC。则下列说法正确的是
A.该反应的化学平衡常数表达式是K=
B.增加B,平衡向右移动,B的平衡转化率增大
C.此时,B的平衡转化率是40%
D.增大该体系的压强,平衡向右移动,化学平衡常数增大
C
解析试题分析:A由于固体物质的浓度在反应中不变,所以该反应的化学平衡常数表达式是K=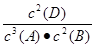 ,错误。B增大反应物的浓度,平衡向正反应方向移动,使其它反应物转化率提高;但对该物质来说平衡移动消耗的该物质远远小于增加的该物质,所以这种物质的转化率反而降低。错误。C根据化学方程式可知生成1.6molC,消耗B 0.8mol。则它的转化率是:0.8∕2×100℅=40%.正确。D对于一个确定的化学反应来说,化学平衡常数只与温度有关。错误。
,错误。B增大反应物的浓度,平衡向正反应方向移动,使其它反应物转化率提高;但对该物质来说平衡移动消耗的该物质远远小于增加的该物质,所以这种物质的转化率反而降低。错误。C根据化学方程式可知生成1.6molC,消耗B 0.8mol。则它的转化率是:0.8∕2×100℅=40%.正确。D对于一个确定的化学反应来说,化学平衡常数只与温度有关。错误。
考点:考查化学平衡常数的表达式、反应物的转化率的计算、外界条件对化学平衡的影响等的知识。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知A(s)+2B(g)  2C(g)+D(g) △H<0 在一密闭容器中反应的υ-t图。t1时,改变了一个条件,下列叙述正确的是
2C(g)+D(g) △H<0 在一密闭容器中反应的υ-t图。t1时,改变了一个条件,下列叙述正确的是
| A.t1时,一定是升高了反应的温度 |
| B.t1时,可能是向容器中通入了一定量的C气体 |
| C.t1时,可能是向容器中加入了催化剂 |
| D.t1时改变外界条件后,该反应的平衡常数可能减小,也可能不变 |
下列措施肯定能使化学反应速率增大的是
| A.增大反应物的量 | B.增加压强 | C.升高温度 | D.使用催化剂 |
化学反应C(s)+H2O(g) CO(g)+H2(g);△H>0达到平衡,下列叙述正确的是
CO(g)+H2(g);△H>0达到平衡,下列叙述正确的是
| A.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
| B.加入固体碳,平衡向正反应方向移动 |
| C.加入水蒸气使容器压强增大,平衡向逆反应方向移动动 |
| D.减小压强,平衡向正反应方向移 |
下列条件:①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积 ④不断分离出生成物 ⑤加入MnO2,一定能使反应速率增大的是
| A.② | B.②③ | C.①②⑤ | D.全部 |
对于可逆反应2HI(g)  I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是
I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是
| A.各物质的量的浓度比2 : 1: 1 |
| B.容器内的总压不随时间变化 |
| C.生成2 mol H-I键的同时生成1 mol I-I键 |
| D.混合气体的颜色不再变化时 |

 ?C达到平衡后,B的转化率与压强、温度的关系如图所示。下列说法正确的是( )
?C达到平衡后,B的转化率与压强、温度的关系如图所示。下列说法正确的是( )