��Ŀ����
������Ԫ��X��Y��Z��W ��ԭ����������������ԭ������������֮��Ϊ13��X ��ԭ�Ӱ뾶��Y ��С��X ��W ͬ���壬Z �ǵؿ��к�����ߵ�Ԫ�ء�����˵����ȷ����
| A��ԭ�Ӱ뾶�Ĵ�С˳��: r(Y)��r(Z)��r(W) |
| B��Ԫ��Z��W �ļ����ӵĵ��Ӳ�ṹ��ͬ |
| C��Ԫ��Y �ļ���̬�⻯������ȶ��Ա�Z ��ǿ |
| D��ֻ��X��Y��Z ����Ԫ�صĻ�������������ӻ����Ҳ�����ǹ��ۻ����� |
D
�������������������Ԫ��X��Y��Z��W ��ԭ��������������Z �ǵؿ��к�����ߵ�Ԫ�أ�ZΪ��Ԫ�أ�X ��ԭ�Ӱ뾶��Y ��С����X��������Y����ͬһ���ڣ�Y��ԭ������С����Ԫ�أ���Y���ڵڶ����ڣ�X���ڵ�һ���ڣ���XΪ��Ԫ�أ�X��Wͬ���壬��WΪNaԪ�أ���ԭ������������֮��Ϊ13����Yԭ�ӵ�����������Ϊ13-1-1-6=5����YΪ��Ԫ�أ�A��ͬ����������ң�ԭ�Ӱ뾶��С��ͬ�������϶���һ���Ӱ뾶����ԭ�Ӱ뾶Na��N��O����r��W����r��Y����r��Z����A����B��O2����Na�����ӵĺ������������10�����ӣ�������Ӳ�ṹ��ͬ��B����C��ͬ����������ҷǽ�������ǿ���ʷǽ�����O��N���ǽ�����Խǿ��̬�⻯��Խ�ȶ������⻯���ȶ���H2O��NH3��C����D����H��N��O��Ԫ����ɵĻ������У�������Ϊ���ۻ���������Ϊ���ӻ����D��ȷ��ѡD��
���㣺λ�ýṹ���ʵ����ϵӦ��

���ǵ�4���ڵڢ�A��ǽ���Ԫ�أ����й�������Ʋⲻ��ȷ���ǣ� ��
| A�����ڶ�����Ԫ�� | B�����Դ��ڣ�3��+3��+5�ȶ��ֻ��ϼ� |
| C������ͨ��������ǹ��� | D�����������As2O5�������������� |
��֪33As��35Brλ��ͬһ���ڣ����й�ϵ��ȷ���� ( )
| A��ԭ�Ӱ뾶��As��C1��P | B�����ȶ��ԣ�HC1��AsH3��HBr |
| C����ԭ�ԣ�As3-��S2-��C1- | D�����ԣ�H3AsO4��H2SO4��H3PO4 |
X��Y��Z��WΪ���ֶ���������Ԫ�أ����������ڱ��е����λ����ͼ��ʾ��ZԪ��ԭ�Ӻ���K����M���������ȡ�����˵������ȷ����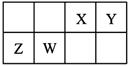
| A��YԪ������������Ӧ��ˮ���ﻯѧʽΪH2YO3 |
| B��ԭ�Ӱ뾶��С�����˳��Ϊ��Y��X��W��Z |
| C�������£�Z��W�ĵ��ʾ�������Ũ���� |
| D��X��Z����Ԫ�ص���������������ѧ��������ͬ |
������ʵ�У����������ж�Ԫ��ʧ��������ǿ������
| A�������䷢�����û���Ӧ |
| B������Ԫ�ص�����������Ӧˮ����ļ���ǿ�� |
| C������Ԫ�صĵ�����ˮ���ᷴӦ�û������������� |
| D��ÿĦ�����������ڷ�Ӧ��ʧȥ������Ŀ�Ķ��� |
�ݱ�����ijЩ�������ϻ�����������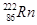 ���Ӷ�����������˺�����ԭ�ӵ���������������֮����
���Ӷ�����������˺�����ԭ�ӵ���������������֮����
| A��136 | B��50 | C��86 | D��222 |
X��Y��Z��W��Ԫ�����ڱ���ԭ������������������ֶ�����Ԫ�أ��������Ϣ���±���
| Ԫ�� | �����Ϣ |
| X | ơ�ƺ������г�����X������������ƿ��ʱ�����������������ݳ� |
| Y | Y2�ǿ����к�����ߵ����嵥�� |
| Z | Z�Ļ�̬ԭ�����������Ų�ʽΪ2s22p4 |
| W | W��һ�ֺ���������Ϊ27��������Ϊ14 |
��1��Wλ��Ԫ�����ڱ��� ���ڵ� �壻Z��W��������Ӱ뾶��С��ϵΪ
�������ӷ��ű�ʾ��
��2��һ��X�γɵĵ��ʣ�����Ȼ��Ӳ���������ʣ����ۻ����ֵ��ʣ�����˷���������������� ��Y�ĵ縺�Ա�Z �����С����
��3��W�ĵ�����NaOH��Һ��Ӧ�����ӷ���ʽΪ �� W�ڸ��������¿ɻ�ԭ���۵�Ľ����������ƵĽ������ʣ�д��W��ԭCr2O3��Ӧ�Ļ�ѧ����ʽ�� ��
��4��úȼ�ղ�������������Y����������������صĻ������⣬��ˣ�����XH4����ԭ��������Ⱦ����֪��
XH4(g)+2 YO2(g)="=" Y2(g)+ XO2(g)+2H2O (g) ��H1= -867kJ/mol
2 YO2(g)
 Y2O4(g) ��H2=-56.9kJ/mol
Y2O4(g) ��H2=-56.9kJ/mol �й�����˵����ȷ����
| A����ԭ��X��������Ϊa����X��������һ����Ϊa |
| B��������Ԫ���γɵ�����M2����N�����Ӳ�ṹ��ͬ�������Ӱ뾶M2��>N�� |
| C��ͬ���ڷǽ����������Ӧˮ�������Դ�����������ǿ |
| D��������Ԫ����ɵĻ�������������Ӽ�����û�й��ۼ� |