题目内容
12.某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA-?H++A2-,关于下列说法不正确的是( )| A. | NaHA的水溶液可能呈酸性,也可能呈碱性 | |
| B. | 0.1mol•L-1Na2A溶液中,c(A2-)+c(HA-)=0.1 mol•L-1 | |
| C. | NaHA的水溶液中离子浓度关系为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| D. | Na2A的水溶液中:c(Na+)=2c(HA-)+2c(A2-) |
分析 A.由于H2A的第一步电离完全进行,则HA-离子在溶液中只能电离,不发生水解,其溶液显示酸性;
B.根据0.1mol•L-1Na2A溶液中的物料守恒分析;
C.根据A可知,溶液中HA-部分电离,溶液显示酸性,溶液中氢离子还来自水的电离,则c(H+)>c(A2-)>c(OH-);
D.Na2A中HA-离子不水解,根据Na2A溶液中的物料守恒分析.
解答 解:A.根据H2A=H++HA-、HA-?H++A2-可知第一步电离进行完全,则HA-离子在溶液中只电离不水解,则NaHA溶液显示酸性,故A错误;
B.0.1mol•L-1Na2A溶液中,根据物料守恒可得:c(A2-)+c(HA-)=0.1 mol•L-1,故B正确;
C.根据A可知,NaHA溶液显示酸性,则c(H+)>c(OH-),由于溶液中氢离子来自HA-和水的电离,则c(H+)>c(A2-),溶液中离子浓度大小为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),故C正确;
D.Na2A中HA-离子不水解,则溶液中不存在H2A分子,根据Na2A的水溶液中的物料守恒可得:c(Na+)=2c(HA-)+2c(A2-),故D正确;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确该二元弱酸的第一步电离进行完全为解答关键,注意掌握电荷守恒、物料守恒及盐的水解原理在判断离子浓度大小中应用方法.

练习册系列答案
相关题目
2.下列说法正确的是( )
| A. |  的名称为2-甲基-2-丙醇 的名称为2-甲基-2-丙醇 | |
| B. | 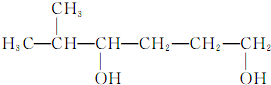 的名称为2-甲基-3,6-己二醇 的名称为2-甲基-3,6-己二醇 | |
| C. | 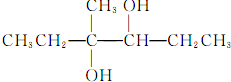 的名称为4-甲基-2,4己-二醇 的名称为4-甲基-2,4己-二醇 | |
| D. | 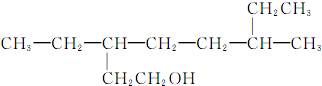 的名称为3,6-二乙基-1-庚醇 的名称为3,6-二乙基-1-庚醇 |
3.在容积不变的密闭容器中进行如下反应:H2O(g)+C(s)?H2(g)+CO(g)△H>0 达到平衡后,只改变下列反应条件,相关叙述正确的是( )
| A. | 加入H2O(g),平衡向正反应方向移动,体系压强减小 | |
| B. | 加入CO,混合气体的密度增大 | |
| C. | 降低温度,平衡向正反应方向移动 | |
| D. | 加入少量C,正反应速率增大 |
20. 将漫射日光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上(如图).现列出如下现象,其中正确的是( )
将漫射日光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上(如图).现列出如下现象,其中正确的是( )
①试管内黄绿色逐渐消失 ②试管内黄绿色加深
③无任何现象④试管内液面上升⑤试管内壁上有油状物生成.
 将漫射日光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上(如图).现列出如下现象,其中正确的是( )
将漫射日光照射到装有氯气和甲烷混合气体(体积比为4:1)的装置上(如图).现列出如下现象,其中正确的是( )①试管内黄绿色逐渐消失 ②试管内黄绿色加深
③无任何现象④试管内液面上升⑤试管内壁上有油状物生成.
| A. | ① | B. | ①④和⑤ | C. | ①和⑤ | D. | ②和⑤ |
17.关于如图所示转化关系(X代表卤素),说法不正确的是( )
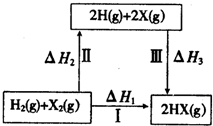

| A. | 2H(g)+2X(g)═2HX(g)△H3<0 | |
| B. | 途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3 | |
| C. | 途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定 | |
| D. | Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多 |
4.奠定近代化学基础的学说是( )
| A. | 分子-原子论 | B. | 元素周期律 | C. | 物质不灭定律 | D. | 质量守恒定律 |
 .
.