题目内容
4.奠定近代化学基础的学说是( )| A. | 分子-原子论 | B. | 元素周期律 | C. | 物质不灭定律 | D. | 质量守恒定律 |
分析 化学的发展史可分为三个阶段:古代化学、近代化学、现代化学,在古代对化学的认识只停留在表象阶段,到了近代,道尔顿和阿伏加德罗创立了原子论-分子学说,奠定了近代化学的基础.
解答 解:A、分子-原子论的创立是认识和分析化学现象及本质的基础,是奠定了近代化学基础的理论,故A正确;
B、元素周期律的发现使化学的学习和研究变得有规律可循,不是奠定近代化学基础的理论,故B错误;
C、物质不灭定律,不是奠定近代化学基础的理论,故C错误;
D、质量守恒定律,揭示了物质发生化学反应时的质量关系,不是奠定近代化学基础的理论,故D错误.
故选A.
点评 本题难度不大,考查化学发展的历史,通过本题的解答有利于激发学生学习化学的兴趣,培养社会责任感.

练习册系列答案
相关题目
14.满足相应条件的下列有机物,同分异构体数目最少的是( )
| 选项 | 分子式 | 结构或性质 |
| A | C5H10 | 能使溴的CCl4溶液褪色 |
| B | C7H7Br | 含甲基和苯环 |
| C | C5H12O | 能与Na反应生成H2 |
| D | C5H10O2 | 能与碳酸氢钠反应生成CO2 |
| A. | A | B. | B | C. | C | D. | D |
12.某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA-?H++A2-,关于下列说法不正确的是( )
| A. | NaHA的水溶液可能呈酸性,也可能呈碱性 | |
| B. | 0.1mol•L-1Na2A溶液中,c(A2-)+c(HA-)=0.1 mol•L-1 | |
| C. | NaHA的水溶液中离子浓度关系为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| D. | Na2A的水溶液中:c(Na+)=2c(HA-)+2c(A2-) |
19.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1.7g羟基含有的电子数目为NA | |
| B. | 常温常压下,23g由NO2与N2O4组成的混合气体含有的氮原子数目为0.5NA | |
| C. | 标准状况下,6.72L H2O中含有的水分子数目为0.3NA | |
| D. | 1 mol•L-1NaClO溶液中含有的ClO-数目为NA |
9.已知氮元素和氧元素组成的化合物中 氮元素和氧元素的质量比为7:16其化学式可能为( )
| A. | NO | B. | NO2 | C. | N2O | D. | N2O5 |
16.下列说法能用质量守恒定律解释的是( )
| A. | mg水受热变为mg的水蒸气 | |
| B. | 62g磷和80g氧气反应生成142g五氧化二磷 | |
| C. | 20g食盐溶于80g水得到100g的食盐水 | |
| D. | 拧开盛酒精的瓶盖一段时间后质量变小 |
14.下列粒子的空间构型不是正四面体的是( )
| A. | SiH4 | B. | CH3Cl | C. | P4 | D. | NH4+ |
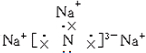 ;该化合物是由离子键形成的离子(填“离子”或“共价”)化合物.
;该化合物是由离子键形成的离子(填“离子”或“共价”)化合物.