题目内容
2.下列事实中一定不能证明CH3COOH是弱电解质的是( )①常温下某CH3COONa溶液的pH②用CH3COOH溶液做导电实验,灯泡很暗
③等pH、等体积的盐酸、CH3COOH溶液和足量锌反应,CH3COOH放出的氢气较多
④0.1mol•L-1CH3COOH溶液的pH=2.1
⑤CH3COONa和H3PO4反应,生成CH3COOH
⑥0.1mol•L-1的CH3COOH溶液稀释100倍,pH<3.
| A. | ② | B. | ②⑤ | C. | ①③⑤ | D. | ③④⑤⑥ |
分析 可通过以下角度证明CH3COOH是弱电解质:
①证明醋酸部分电离;
②证明醋酸存在电离平衡;
③测定对应强碱盐的酸碱性;
④证明醋酸根离子存在水解平衡;
⑤强酸能够制取弱酸;
⑥证明醋酸加水稀释时能够继续电离,存在电离平衡.
解答 解:①常温下某CH3COONa溶液的pH=8,说明溶液水解呈碱性,应为强碱弱酸盐,可证明CH3COOH是弱电解质,故①正确;
②用CH3COOH溶液做导电实验,灯泡很暗,不能证明CH3COOH是弱电解质,只能说明溶液离子浓度较小,故②错误;
③等pH等体积的盐酸、CH3COOH溶液和足量锌反应,CH3COOH放出的氢气较多,说明醋酸还可电离出氢离子,可证明CH3COOH是弱电解质,故③正确;
④0.1mol•L-1 CH3COOH溶液的pH=2.1,说明醋酸没有完全电离,可以证明CH3COOH是弱电解质,故④正确;
⑤CH3COONa和H3PO4反应,生成CH3COOH,说明醋酸的酸性比磷酸弱,而磷酸为中强酸,则醋酸为弱酸,故⑤正确;
⑥0.1mol•L-1的CH3COOH溶液稀释至100倍,pH<3,说明存在电离平衡,证明CH3COOH是弱电解质,故⑥正确.
故选A.
点评 本题考查弱电解质的电离,题目难度中等,明确实验证明的角度为解答该题的关键,注意体会实验方案的合理性.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
12.某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA-?H++A2-,关于下列说法不正确的是( )
| A. | NaHA的水溶液可能呈酸性,也可能呈碱性 | |
| B. | 0.1mol•L-1Na2A溶液中,c(A2-)+c(HA-)=0.1 mol•L-1 | |
| C. | NaHA的水溶液中离子浓度关系为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| D. | Na2A的水溶液中:c(Na+)=2c(HA-)+2c(A2-) |
10.20℃时,NaCl溶解于水的实验数据如下表所示
下列叙述正确的是( )
| 实验序号 | 水的质量/g | 加入的NaCl质量/g | 未溶的NaCl质量/g |
| ① | 10 | 2 | 0 |
| ② | 10 | 3 | 0 |
| ③ | 10 | 4 | 0.4 |
| A. | 实验①所得的溶液为饱和溶液 | |
| B. | 实验②所得的溶液为饱和溶液 | |
| C. | 20℃时NaCl的溶解度为30g | |
| D. | 实验①所得溶液的溶质质量分数为16.7% |
7.2013年12月5日中国辽宁舰航母编队中的登陆舰紧急逼停了擅闯南海禁航区的美海军“考本斯”号导弹巡洋舰,避免了两军舰艇相撞.据悉,美国“考本斯”号巡洋舰上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)做载热介质.下列有关说法不正确的是( )
| A. | 自然界中没有游离的钠和铝 | |
| B. | 若铝钠合金投入水中得无色溶液,则n(Al)≤n(Na) | |
| C. | 铝钠合金投入到水中,一定有偏铝酸钠生成 | |
| D. | m g不同组成的铝钠合金投入足量盐酸中,若放出的H2越多,则铝的质量分数越小 |
14.下列粒子的空间构型不是正四面体的是( )
| A. | SiH4 | B. | CH3Cl | C. | P4 | D. | NH4+ |
11.水杨酸环已酯具有花香气味,可作为香精配方.其合成路线如图:
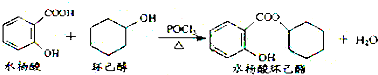
下列说法正确的是( )

下列说法正确的是( )
| A. | 水杨酸能分别与NaHCO3、Na2CO3溶液反应,且1 mol水杨酸分别消耗NaHCO32mol、Na2CO31mol | |
| B. | 水杨酸、环己醇和水杨酸环己酯均能与FeCl3溶液发生显色反应 | |
| C. | 1 mol水杨酸环己酯在NaOH溶液中水解时,最多消耗3 mol NaOH | |
| D. | 1 mol水杨酸跟足量浓溴水反应时,最多消耗Br2 2 mol |
12. 在容积为10L的密闭容器中通入一定量的SO2和O2,450℃时发生反应:2SO2+O2?2SO3(正反应放热),SO2和O2的物质的量浓度随反应时间的变化如图所示.请回答下列问题:
在容积为10L的密闭容器中通入一定量的SO2和O2,450℃时发生反应:2SO2+O2?2SO3(正反应放热),SO2和O2的物质的量浓度随反应时间的变化如图所示.请回答下列问题:
(1)0~4min的平均反应速率v(SO2)=0.03mol•L-1•min-1.
(2)在其他条件不变,7min时分别改变下列条件,将改变条件的瞬间正反应速率的变化情况(“增大”、“减小”或“不变”)填入表空格内:
 在容积为10L的密闭容器中通入一定量的SO2和O2,450℃时发生反应:2SO2+O2?2SO3(正反应放热),SO2和O2的物质的量浓度随反应时间的变化如图所示.请回答下列问题:
在容积为10L的密闭容器中通入一定量的SO2和O2,450℃时发生反应:2SO2+O2?2SO3(正反应放热),SO2和O2的物质的量浓度随反应时间的变化如图所示.请回答下列问题:(1)0~4min的平均反应速率v(SO2)=0.03mol•L-1•min-1.
(2)在其他条件不变,7min时分别改变下列条件,将改变条件的瞬间正反应速率的变化情况(“增大”、“减小”或“不变”)填入表空格内:
| 改变的条件 | v正 | v逆 |
| ①减小SO2的浓度 | 减小 | 不变 |
| ②减小SO3的浓度 | 不变 | 减小 |
| ③缩小容器的体积 | 增大 | 增大 |
| ④加入V2O5作催化剂 | 增大 | 增大 |