题目内容
【题目】溶液X中含有右表离子中的某5种,且其浓度均为![]() 不考虑水的电离与离子水解
不考虑水的电离与离子水解![]() 向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化.下列叙述不正确的是( )
向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化.下列叙述不正确的是( )
阳离子 | 阴离子 |
Fe Fe |
|
A.X溶液中不可能含有![]() 或
或![]()
B.生成无色气体的离子方程式为:![]()
C.根据电荷守恒,原溶液中一定含![]()
D.X溶液中一定含3种阳离子、2种阴离子
【答案】D
【解析】
各种离子的物质的量浓度均为![]() ,向溶液X中加入足量的盐酸,有气体生成,且反应溶液中阴离子的种类没有变化,产生气体不可能是碳酸根离子或碳酸氢根离子;根据表中的离子,可推知是
,向溶液X中加入足量的盐酸,有气体生成,且反应溶液中阴离子的种类没有变化,产生气体不可能是碳酸根离子或碳酸氢根离子;根据表中的离子,可推知是![]() 、
、![]() 在酸性环境下生成的一氧化氮,加入盐酸,溶液中阴离子种类不变,所以原来溶液中含有
在酸性环境下生成的一氧化氮,加入盐酸,溶液中阴离子种类不变,所以原来溶液中含有![]() ,若只含有氯离子和硝酸根离子,二者的浓度为
,若只含有氯离子和硝酸根离子,二者的浓度为![]() ,根据电荷守恒是不可能的,所以还含有阴离子
,根据电荷守恒是不可能的,所以还含有阴离子![]() ,由于总共含有5种离子,再根据电荷守恒可知还含有一种带有两个正电荷的
,由于总共含有5种离子,再根据电荷守恒可知还含有一种带有两个正电荷的![]() ,所以原溶液中含有的五种离子为:
,所以原溶液中含有的五种离子为:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,
,
A.根据分析可知,溶液中一定不存在![]() 与
与![]() ,故A正确;
,故A正确;
B.生成无色气体为NO,反应的离子方程式为:![]() ,故B正确;
,故B正确;
C.原溶液中一定含有![]() ,故C正确;
,故C正确;
D.原溶液中含有的五种离子为:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,含有2种阳离子、3种阴离子,故D错误;
,含有2种阳离子、3种阴离子,故D错误;
故选:D。

【题目】水溶液中的离子平衡是中学学习的一个重要内容。
(1)甲同学用pH试纸分别测定了 0.1 mol/L NaOH溶液的pH=13、0.1 mol/LCH3COOH溶液的pH=3、0.001 mol/L HCl溶液的pH=3。请写出pH试纸使用方法:_____根据测量结果,甲推测等浓度的NaOH溶液、CH3COOH溶液中,由水电离出的H+浓度c(H+)NaOH____c(H+)CH3COOH(填“大于”“小于”或“等于”)
(2)乙同学分别取了pH=3的CH3COOH溶液和HCl溶液各10mL,测量导电能力发现HCl溶液导电能力______________CH3COOH溶液导电能力(填“大于”“小于”或“等于”)。然后分别加水稀释到100 mL后,再次测量,稀释后的HCl溶液导电能力______________CH3COOH溶液导电能力(填“大于”“小于”或“等于”)
(3)丙同学查阅资料发现,人体血液里存在重要的酸碱平衡:CO2+H2O![]() H2CO3
H2CO3![]() HCO3-,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
HCO3-,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随c(HCO3-)∶c(H2CO3)变化关系如下表:
c(HCO3-) ∶c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
pH | 6.10 | 7.35 | 7.40 | 7.45 |
①正常人体血液中,HCO3-的水解程度____电离程度(填“>”、“<”或“=”);
②人体血液酸中毒时,可注射________(填选项)缓解;
A.NaOH溶液 B.NaHCO3溶液 C.NaCl溶液 D.Na2SO4溶液
③等浓度的Na2CO3和NaHCO3的混合溶液中各离子浓度大小顺序___________
④已知25 ℃时,CO32-水解反应的平衡常数Kh=![]() =
=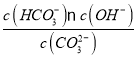 =2×10-4 mol/L,当溶液中c(HCO3-)︰c( CO32-)=2:1时,溶液的pH=________;
=2×10-4 mol/L,当溶液中c(HCO3-)︰c( CO32-)=2:1时,溶液的pH=________;
(4)丁同学探究难溶电解质在水溶液中的性质,查阅资料发现25 ℃时,AgCl的Ksp=1.8×10-10,该温度下向1 L 0.03 mol/L的AgNO3溶液中加入1 L 0.01 mol/L的NaCl溶液之后,溶液中c(Cl-)=______mol/L(忽略混合前后溶液体积的变化)。平衡后,若向该体系中再加入少量AgCl固体,则c(Cl-)_____(填“增大”或“减小”或“span>不变”)。