题目内容
【题目】下列有关SO2的说法中,不正确的是
A.溶于水能导电,属于电解质
B.使品红溶液褪色,有漂白性
C.使酸性高锰酸钾溶液褪色,有还原性
D.能杀菌、消毒,可按照国家标准用作食物的防腐剂
【答案】A
【解析】
试题分析:A.二氧化硫能溶于水,溶解后生成的亚硫酸能够电离,溶液能导电,但二氧化硫属于非电解质,错误;B.二氧化硫能使品红溶液褪色,体现了二氧化硫的漂白性,正确;C.二氧化硫能使酸性高锰酸钾溶液褪色,体现了二氧化硫的还原性,正确;D.二氧化硫有毒,能杀菌、消毒,可按照国家标准用作食物的防腐剂,正确;故选A。

【题目】某小组同学在实验室里对Fe3+与I﹣的反应进行探究,实现Fe3+与Fe2+相互转化.
(1)甲同学首先进行了如下实验:
编号 | 操作 | 现象 |
Ⅰ | 先向2mL0.1molL﹣1FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | ___________________ ___________________ |
Ⅱ | 先向2mL0.1molL﹣1FeCl3溶液中滴加KSCN溶液,再滴加0.1molL﹣1KI溶液 | 滴加KSCN溶液后,溶液变成血红色;滴加0.1molL﹣1KI溶液后,血红色无明显变化 |
实验Ⅰ中发生反应的离子方程式为 , .
(2)实验II的现象与预测不同,为探究可能的原因,甲同学又进行了如下实验,
操作及现象如下:
编号 | 操作 | 现象 |
Ⅲ | 向2mL0.1molL﹣1KI溶液中滴加1mL 0.1molL﹣1FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成血红色 |
根据实验Ⅲ,该同学认为Fe3+有可能与I﹣发生氧化还原反应.请结合实验现象说明得出该结论的理由: .
(3)乙同学认为,还需要进一步设计实验才可证明根据实验Ⅲ中现象得出的结论.
请补全下表中的实验方案:
编号 | 操作 | 预期现象及结论 |
Ⅳ | 向2mL0.1molL﹣1KI溶液中滴加1mL 0.1molL﹣1 FeCl3,溶液变黄色,取该溶液于两支试管中, 试管①中滴加 , 试管②中滴加 . | 预期现象① , ② . 结论 . |
(4)上述实验结果表明,Fe3+有可能与I﹣发生氧化还原反应.进一步查阅资料知,参加反应的Fe3+和I﹣物质的量相同.该小组同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变血红色的原因,认为Fe3+与I﹣反应的离子方程式应写为: .
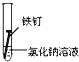
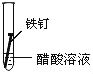
【题目】全世界每年因钢铁锈蚀造成大量的损失.某学生欲探究在蒸馏水、氯化钠溶液和醋酸溶液三种条件下铁锈蚀的快慢,设计了如表实验.
实验序号 | Ⅰ | Ⅱ | Ⅲ |
实验 内容 |
|
|
|
请回答:
①在一周的观察过程中,他发现实验序号为 的试管中铁钉锈蚀速度最慢..
②下列防止钢铁锈蚀的措施不合理的是 (填字母).
A.在自行车的钢圈表面镀镍
B.改变金属内部结构制成不锈钢.
C.在地下钢铁管道上连接铜块
③炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑.试回答:铁锅的腐蚀主要是由 腐蚀造成的.