题目内容
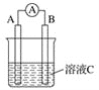
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。下列有关说法正确的是( )

A.反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B.乙装置中铁电极为阴极,电极反应式为Fe-2e-=Fe2+
C.甲中通入氧气的一极为阳极,发生的电极反应为O2+4e-+2H2O=4OH-
D.反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
【答案】A
【解析】
燃料电池中,投放燃料的电极是负极,投放氧化剂的电极是正极,则Fe为阴极,C为阳极,精铜为阴极,粗铜为阳极;
A.乙中Fe为阴极,阴极上氢离子放电生成氢气和氢氧根离子,所以乙装置中生成的氢氧化钠在铁极区,故A正确;
B.乙装置中铁电极为阴极,阴极上溶液中的阳离子得电子,则阴极电极方程式为2H++2e-═H2↑;故B错误;
C.甲装置为原电池装置,原电池中没有阳极,故C错误;
D.阳极上活泼性比铜强的金属先失电子,阴极上只有铜离子得电子,由于两极上得失电子守恒,所以溶解的Cu与生成的Cu不相同,则溶液中铜离子浓度减小,故D错误。
故选:A。

练习册系列答案
相关题目