题目内容
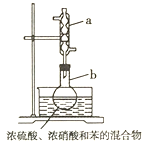
【题目】某化学兴趣小组的同学欲除去固体氯化钠中混有的氯化钙,请据如下实验方案回答问题。
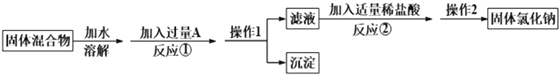
(1)操作1的名称是_____;
(2)反应①中加入略过量的A物质的目的是__________;
(3)写出反应②的化学方程式:_______。
(4)实验时称取样品的质量为185.0g,经过操作1后,测得沉淀(不溶于水)的质量为50.0g, 则样品中NaCl的质量分数是多少___?(写出计算过程)
【答案】过滤 保证钙离子沉淀完全 Na2CO3+2HCl=2NaCl+CO2↑+H2O 70%
【解析】
(1)由分离流程可知,溶解后加过量的Na2CO3可除去氯化钙,操作①为过滤,得到沉淀为碳酸钙,滤液中含NaCl、Na2CO3,加适量盐酸,与碳酸钠反应,操作②为蒸发,最后得到NaCl, 操作1的名称是过滤;
答案为:过滤。
反应①中加入略过量的A物质的目的是保证钙离子沉淀完全;判断A已过量的实验操作方法是静置后取少量上层清液,滴加适量的稀盐酸,若上层有气体,则说明碳酸钠已过量,答案为:保证钙离子沉淀完全;
(3)反应②的化学方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O,因盐酸易挥发,如果加入盐酸过量,则对所得到的氯化钠的纯度没有影响,
答案为:Na2CO3+2HCl=2NaCl+CO2↑+H2O;
(4)经过操作1后,测得沉淀(不溶于水)的质量为50.0g,根据钙原子守恒,则n(CaCl2)=n(CaCO3)=![]() =0.5mol,则样品中NaCl的质量分数是
=0.5mol,则样品中NaCl的质量分数是![]() ×100%=70%,
×100%=70%,
答案为:70%。

【题目】亚硝酰氯(ClNO)是有机合成中的重要试剂,可通过反应:2NO(g)+Cl2(g)2ClNO(g)获得。
(1)氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
①2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g)![]() 2ClNO(g) K3
2ClNO(g) K3
则K3=__________(用K1、K2表示)。
(2)300℃时,2NO(g)+Cl2(g)2ClNO(g)的正反应速率表达式为v(正)=k·cn(ClNO),测得速率和浓度的关系如表所示:
序号 | c(ClNO)/(mol/L) | v/(x10-8mol·L-1·S-1) |
① | 0.30 | 0.36 |
② | 0.60 | 1.44 |
③ | 0.90 | 3.24 |
k=__________________________。
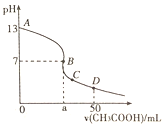
(3)按投料比[n(NO):n(Cl2)=2:1]把 NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图A所示:
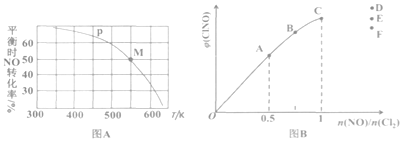
①在p压强条件下,M点时容器内NO的体积分数为______________。
②若反应一直保持在P压强条件下进行,则M点的分压平衡常数KP=________(用含P的表达式表示,用平衡分压代替平衡浓度计算,分压=总压 x体积分数)。
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2)的变化图像如图B所示,则A、B、C三状态中,NO的转化率最大的是________点,当n(NO)/n(Cl2)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的_______点。