题目内容
【题目】在![]() 某一元碱(
某一元碱(![]() )中,滴加入
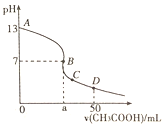
)中,滴加入![]() 的醋酸溶液,滴定曲线如图所示。下列说法错误的是( )
的醋酸溶液,滴定曲线如图所示。下列说法错误的是( )
A.该碱溶液可以溶解![]()
B.![]() 点对应的体积大于
点对应的体积大于![]()
C.![]() 点时,
点时,![]()
D.![]() 点时,
点时,![]()
【答案】D
【解析】
A. 由A点知:0.1molL1一元碱的pH=13可得,该碱为强碱,所以该碱溶液可以溶解![]() ,故A正确;
,故A正确;
B. 恰好中和时生成强碱弱酸盐pH应大于7,而B点pH=7,所以该点对应的溶质为CH3COOY和CH3COOH,a点的体积大于25mL,故B正确;
C. C点对应的溶质为CH3COOY和CH3COOH,溶液中CH3COOY的浓度>CH3COOH的浓度,因pH<7,所以c(H+)>c(OH),弱酸的电离是微弱的,结合电荷守恒c(CH3COO)+c(OH)=c(H+)+c(Y+),则应有c(CH3COO)>c(Y+)> c(H+)>c(OH),故C正确;
D. D点为CH3COOY和CH3COOH等物质的量浓度的混合液,根据物料守恒c(CH3COO)+c(CH3COOH)=2c(Y+)和电荷守恒c(CH3COO)+c(OH)=c(H+)+c(Y+),所以应有![]() ,故D错误;
,故D错误;
答案选D。

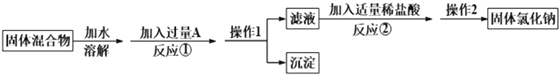
【题目】某班几个兴趣小组做了以下实验。
甲组:两同学利用下列试剂:铁粉、0.1mol/L FeCl3溶液、0.1mol/L FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+ 的性质,设计实验方案进行实验,完成下列表格。
探究内容 | 实验方案 | 实验现象 | 写出离子方程式 |
①探究Fe2+具有还原性 | 取少FeCl2溶液,加入少量KSCN溶液后,再往溶液中加入少量________。 | 溶液先不变红,后变为血红色。 | Fe2+发生的反应: _____________ |
②探究Fe3+具有氧化性 | 取少量FeCl3溶液,加入足 量______后,振荡,静置,再往溶液中加入少量KSCN溶液。 | 溶液不变为血红色。 | Fe3+发生的反应:________ |
乙组:两同学利用下图所示的装置进行铁与水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
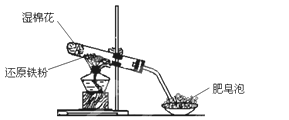
请回答下列问题。
(1)硬质试管中发生反应的化学方程式为_______________。
(2)欲确定反应后硬质试管中固体物质的成分,实验过程如下:
①待硬质试管冷却后,取少许其中的固体物质溶于足量稀硫酸得溶液B;
②取少量溶液B于试管a中,滴加KSCN溶液,溶液没有变红色,则溶液B中的阳离子有_________________,硬质试管中固体物质的成分是_________________。
(3)另取少量溶液B,使其与NaOH溶液反应(按图所示),在胶头滴管挤出NaOH溶液的瞬间可观察到生成白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色。请写出与上述现象中白色沉淀转化红褐色沉淀的化学方程式________________。
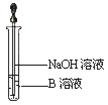
(4)一段时间后,发现a中未变红的溶液变成红色,原因是 _______________
【题目】由下列实验及现象,推出的相应结论正确的是
实验 | 现象 | 结论 |
A.用铂丝蘸取某金属的盐溶液, 在酒精灯火焰上灼烧 | 火焰呈黄色 | 此盐溶液中含有 Na+,不含 K+ |
B.向饱和NaHCO3溶液中加入足量氯水 | 有无色气体产生 | 氯水中含HClO |
C.将足量SO2气体通入石蕊试液中 | 石蕊试液变红色 | SO2水溶液显酸性 |
D.向酸性KMnO4溶液中通入SO2 | 溶液紫色褪去 | SO2具有漂白性 |
A.AB.BC.CD.D