题目内容
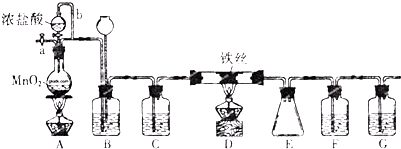
5.单质硅是信息产业中重要的基础材料.通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度为450℃~500℃),四氯化硅经提纯后用氢气还原可得高纯硅.以下是实验室制备四氯化硅的装置图:
相关信息如下:①四氯化硅遇水极易水解
②硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物
③有关物质的物理常数见下表:
| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | -57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
(2)装置A中g管的作用是平衡压强,使液体顺利流出并防止漏气;
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是Al、P(填写元素符号).
(4)甲方案:f接装置Ⅰ;乙方案:f接装置Ⅱ.但是装置Ⅰ、Ⅱ都有不足之处,请你设计一个合理方案并用文字表达:在装置Ⅰ的i处接干燥管j
(5)为了分析残留物中铁元素的含量,先将残留物预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO${\;}_{4}^{-}$+8H+=5Fe3++Mn2++4H2O 某同学称取5.000g残留物,预处理后在容量瓶中配制成100ml溶液,移取25.00ml,试样溶液,用1.000×10-2mol•L-1KMnO4标准溶液滴定.达到滴定终点时,消耗标准溶液20.00ml,则残留物中铁元素的质量分数是4.480%.(写出计算过程)
分析 由制备四氯化硅的实验流程可知,A中发生二氧化锰与浓盐酸的反应生成氯气,B中饱和实验水除去HCl,C装置中浓硫酸干燥氯气,D中发生Si与氯气的反应生成四氯化硅,由信息可知,E装置制取氢气,F可防止倒吸,最后氢气还原SiCl4;
(1)装置A是氯气发生装置,A中的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;根据制得的氯气中含有氯化氢和水,装置B用饱和食盐水除去氯化氢,装置C用浓硫酸吸水;
(2)因浓盐酸有挥发性,故分液漏斗要加盖,加盖后如没有g管,则盐酸就不易流下去,g管的作用是平衡压强,使液体顺利流出并防止漏气;
(3)D中氯气与粗硅反应生成SiCl4,h瓶收集粗产物,精馏粗产品可得高纯度四氯化硅,由表中数据可以看出,蒸出SiCl4气体时,BCl3早已成气体被蒸出,而AlCl3、FeCl3、PCl5升华温度均高于SiCl4;
(4)收集产品的导管太细易堵塞导管;制取的四氯化硅需要冷凝;由于尾气中含有氯气,要设置尾气处理装置,四氯化硅易水解,要避免空气中的水蒸气进入产品收集装置;
(5)结合元素守恒,利用氧化还原反应原理书写离子反应方程式,根据关系式5Fe2+~MnO4-计算出100mL溶液中含有的铁,最后求出质量百分数.
解答 解:(1)装置A是氯气发生装置,A中的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,制得的氯气中含有氯化氢和水,装置B用饱和食盐水除去氯化氢,装置C用浓硫酸吸水;
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;浓硫酸;
(2)浓盐酸有挥发性,故分液漏斗要加盖,加盖后如没有g管,则盐酸就不易流下去,g管的作用是平衡压强,使液体顺利流出并防止漏气;产物SiCl4沸点低,需要冷凝收集;
故答案为:平衡压强,使液体顺利流出并防止漏气;
(3)D中氯气与粗硅反应生成SiCl4,h瓶收集粗产物,精馏粗产品可得高纯度四氯化硅,由表中数据可以看出,蒸出SiCl4气体时,BCl3早已成气体被蒸出,而AlCl3、FeCl3、PCl5升华温度均高于SiCl4的沸点,所以当SiCl4蒸出后,而AlCl3、FeCl3、PCl5还为固体留在瓶里,除铁元素外可能还含有的杂质元素是Al、P,
故答案为:Al、P;
(4)四氯化硅在常温下易液化,如果收集产品的导管太细易堵塞导管;制取的四氯化硅需要冷凝;由于尾气中含有氯气,要设置尾气处理装置,四氯化硅易水解,要避免空气中的水蒸气进入产品收集装置,在装置Ⅰ的i处接干燥管j,
故答案为:在装置Ⅰ的i处接干燥管j;
(5)用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,MnO4-转变成Mn2+溶液颜色有紫色变成无色,KMnO4标准溶液在酸性条件下进行氧化还原滴定时,不需要指示剂,判断是否达到滴定终点的方法为:当滴入最后一滴KMnO4溶液时,溶液颜色由无色变为紫色,且30秒不褪色,利用关系式法计算:
5Fe2+~MnO4-
4×10-3mol 1.000×10-2mol•L-1×0.02L×$\frac{100}{25}$
铁元素的质量为:4×10-3mol×56g/mol=2.24×10-1g,铁元素的质量分数$\frac{2.24×1{0}^{-1}g}{5.000g}$×100%=4.480%,
故答案为:4.480%.
点评 本题为传统的综合实验方案设计题,综合了氯气的制法、硅的提纯、滴定法等了实验知识,注意滴定食盐的定量计算分析,掌握基础是关键,题目难度增中等.

| A. | 氢键有方向性和饱和性,属于共价键 | |
| B. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| C. | 范德华力是一种分子间作用力,也是一种特殊的化学键 | |
| D. | 常温常压下,卤素单质从F2→I2由气态、液态到固态的原因是范德华力逐渐增大 |
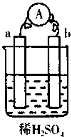
| A. | 碳棒上有气体放出,溶液酸性变弱 | |
| B. | a是正极,b是负极 | |
| C. | 导线中有电子流动,电流从a极到b极 | |
| D. | a极上发生了还原反应 |
| A. | 纯水几乎不导电,因此水是非电解质 | |
| B. | 在任何温度下,纯水的pH均等于7 | |
| C. | 向水中加入钠,溶液中$\frac{{K}_{w}}{c(O{H}^{-})}$减小 | |
| D. | 向水中加入醋酸,c(H+)和水的电离均增大 |
 对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺与浓硫酸(HO-SO3H)磺化得到.实验室可利用右图装置合成对氨基苯磺酸
对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺与浓硫酸(HO-SO3H)磺化得到.实验室可利用右图装置合成对氨基苯磺酸
实验步骤如下:
①在一个250mL三口烧瓶中加入10mL苯胺及少量固体B,把烧瓶放入冷水中,缓慢地加入18mL浓硫酸.
②把三口烧瓶置于油浴中缓慢加热,控制温度为180℃~190℃,反应1~1.5h.
③将反应液冷却至约50℃,倒入盛有100mL冷水的烧杯中,析出灰白色固体,进行操作C并用少量冷水洗涤固体,得到对氨基苯磺酸粗产品.
④对粗产品进行操作D,再低温烘干即得到纯净的对氨基苯甲酸.
以下为两种有机物的部分物理性质,请回答有关问题.
| 苯胺 | 对氨基苯磺酸 | |
| 熔点 | -6.3℃ | 288℃ |
| 沸点 | 184℃ | (300℃开始分解炭化) |
| 水溶性 | 微溶于水 | 微溶于冷水、溶于热水 |
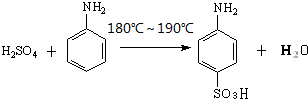 .
.(2)装置A的名称为冷凝管,作用是使苯胺冷凝回流.
(3)固体 B的作用是防暴沸,操作C的名称是过滤.
(4)下列说法正确的是AD
A.用液体加热的好处是反应物受热均匀,便于控制温度
B.本实验步骤②也可以改用水浴加热
C.步骤③将反应液倒入100mL冷水的目的是分离苯胺和对氨基苯磺酸
D.步骤③用少量冷水洗涤的目的是除去固体表面的可溶性杂质同时减少洗涤过程中的损失.
(5)操作D的名称是重结晶,具体过程包括:用适量热水溶解粗产品→冷却结晶→过滤、洗涤.