题目内容
8. (1)将一定量固体A置于一个容器体积不变的密闭容器中发生如下反应:
(1)将一定量固体A置于一个容器体积不变的密闭容器中发生如下反应:A(s)?2B(g)+C(g)在一定温度下达到平衡,则可以判断该反应已经达到平衡的是CD
A﹑v(B)=2v(C)
B﹑密闭容器中的C(g)的体积分数不变
C﹑密闭容器中混合气体的密度不变
D﹑变密闭容器中总压强不变
E﹑密闭容器中混合气体的平均分子量不变
若该反应在升温过程中平衡气体的总浓度是增加的.则该反应的焓变△H>0,熵变△S>O(填>﹑<或者=)
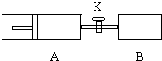
(2)如图,向A充入1molX、1molY,向B中充入2molX、2molY,起始时A、B的体积相等都等于a L,在相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述反应,X(g)+Y(g)?2Z(g)+W(g);△H<0.A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL.则:
①平衡时,Y(g)的体积百分数的大小关系为:B大于A(填大于﹑小于或者等于)
②若打开K一段时间后重新达到平衡,容器A的体积为3.2a(连通管内气体体积忽略不计)
分析 (1)A﹑只要反应发生就符合v(B)=2v(C);
B﹑因为反应物为固体,所以容器中B、C的物质的量之比永远是2:1,所以密闭容器中的C(g)的体积分数始终不变;
C﹑密闭容器中混合气体的密度不变,说明气体的质量不变;
D﹑变密闭容器中总压强不变,说明气体的质量不变;
E﹑密闭容器中混合气体的平均分子量始终不变.
若该反应在升温过程中平衡气体的总浓度是增加的,平衡正向移动,说明正反应是吸热反应;
(2)打开K达新平衡等效为A中到达的平衡,根据X的转化率计算平衡后总的物质的量,再根据体积之比等于物质的量之比计算总体积,进而计算A容器的体积,升高温度,平衡向吸热方向移动,据此判断.
解答 解:(1)A﹑只要反应发生就符合v(B)=2v(C),不能作平衡状态的标志,故错误;
B﹑因为反应物为固体,所以容器中B、C的物质的量之比永远是2:1,所以密闭容器中的C(g)的体积分数始终不变,不能作平衡状态的标志,故错误;
C﹑密闭容器中混合气体的密度不变,说明气体的质量不变,达平衡状态,故正确;
D﹑变密闭容器中总压强不变,说明气体的质量不变,达平衡状态,故正确;
E﹑密闭容器中混合气体的平均分子量始终不变,不能作平衡状态的标志,故错误;
若该反应在升温过程中平衡气体的总浓度是增加的,平衡正向移动,说明正反应是吸热反应,所以△H>0,气体物质的量增加,熵变△S>O,
故答案为:CD;>;>;
(2)①A容器的平衡变化,建立新平衡后,(容积为0.5aL与容积为1.4aL相比)Y的体积分数要减小,即平衡时Y体积分数A<B,故答案为:大于;
②打开K达新平衡等效为A中到达的平衡,X的转化率为80%,参加反应的X的总的物质的量为3mol×80%=2.4mol,则:
X(g)+Y(g)?2Z(g)+W(g) 物质的量增多
1mol 1mol
2.4mol 2.4mol
故平衡后容器内总的物质的量为(1mol+1mol+2mol+2mol)+2.4mol=8.4mol,气体的体积之比等于气体的物质的量之比,则总容器的体积为aL×$\frac{8.4mol}{2mol}$=4.2aL,则A的体积=4.2aL-a=3.2a,故答案为:3.2a.
点评 本题难度较大,需要设计平衡和变换平衡,要求有清晰的思维过程,是一则训练思维的好题.

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案| A. | H2和D2互为同位素 | B. | 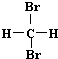 和 和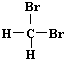 互为同分异构体 互为同分异构体 | ||
| C. | H、D、T互称为同素异形体 | D. | 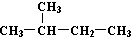 和 和 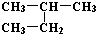 是同一种物质 是同一种物质 |
| A. | 标准状况下,22.4L甲醇中含有的氧原子数为1.0NA | |
| B. | 常温常压下,46gNO2与 N2O4的混合气体中含有的原子总数为3NA | |
| C. | 标准状况下,2.24LCl2与足量的稀NaOH溶液反应,转移电子总数为0.2NA | |
| D. | 1L 1 mol•L-1的盐酸中,所含氯化氢分子数为NA |
| A. | 上述反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | AlN的摩尔质量为41 g | |
| C. | AlN中氮元素的化合价为+3 | |
| D. | 上述反应中,每生成1 mol AlN需转移3 mol电子 |
| 温度/℃ | 25 | T1 | T2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
(1)若25<T1<T2,则a>1×10-14 (填“>”、“<”或“=”),做此判断的理由是水的电离吸热,温度升高,水的电离程度增大,所以水的离子积增大.
(2)25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=1000:1.
(3)T2℃时,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=9:11.此溶液中各种离子的浓度由大到小的顺序是c(Na+)>c(SO42-)>c(H+)>c(OH-).
(4)常温下,设某pH值的硫酸中水电离出的c(H+)=1.0×10-amol/L,设相同pH值的硫酸铝中水电离出的c(H+)=1.0×10-b mol/L,(a、b都是小于14的正数),那么a、b之间满足的关系式是a+b=14.
| A. | 当混合气体的质量不再发生变化时,说明反应达到平衡状态 | |
| B. | 用M表示此反应速率是0.1 a mol•(L•min)-1 | |
| C. | 用X表示此反应的反应速率是(0.1-0.2 a)mol•(L•min)-1 | |
| D. | 其他条件不变向上述平衡体系中再充入lmolX,v(正)增大,v(逆)减小,平衡正向移动 |

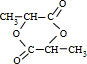 .
.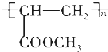 .
.