题目内容
某强酸性溶液中,能大量共存的一组是( )
| A、K+、Na+、AlO2-、SO42- |
| B、NH4+、Na+、I-、NO3- |
| C、Na+、K+、SO42-、CO32- |
| D、Mg2+、Al3+、NO3-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:酸性溶液中含大量的H+,根据离子之间不能结合生成水、气体、沉淀,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答:
解:A.酸性条件下,AlO2-不能大量共存,故A错误;
B.酸性条件下,I-、NO3-发生氧化还原反应而不能大量共存,故B错误;
C.酸性条件下,CO32-不能大量共存,故C错误;
D.酸性条件下,离子之间不发生任何反应,可大量共存,故D正确.
故选D.
B.酸性条件下,I-、NO3-发生氧化还原反应而不能大量共存,故B错误;
C.酸性条件下,CO32-不能大量共存,故C错误;
D.酸性条件下,离子之间不发生任何反应,可大量共存,故D正确.
故选D.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子的反应为解答的关键,侧重氧化还原反应、复分解反应的离子共存考查,选项B为解答的难点,题目难度不大.

练习册系列答案
相关题目
证明氨水是弱碱的事实是( )
| A、氨水与硫酸发生中和反应 |
| B、氨水能使紫色石蕊液变蓝 |
| C、0.1mol/L的NH4Cl溶液的pH值为5.1 |
| D、铵盐与熟石灰反应逸出氨气 |
下列说法正确的是( )
| A、麦芽糖的水解产物能发生银镜反应 |
| B、四氟乙烯(CF2=CF2)中所有的原子都在同一个平面上 |
C、 在酸性条件下水解产物是 在酸性条件下水解产物是 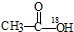 和CH3CH2OH 和CH3CH2OH |
| D、淀粉溶液加适量浓硫酸加热一会儿后,滴入银氨溶液无银镜生成,说明淀粉未水解 |
下列关系正确的是( )
| A、将等物质的量的H2CO3和KHCO3溶于水配成的溶液中:2c(K+)=c(H2CO3)+c(HCO3-) |
| B、向CH3COONa溶液里加入适量的NaOH固体后得到的混合溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C、向0.10mol?L-1 NH4HSO4溶液中滴加适量的NaOH溶液至溶液呈中性,该中性溶液中:c(Na+)>c(SO42-)>c(NH4+)>c(OH-) |
| D、向NaCN溶液中滴加适量的稀盐酸使溶液呈中性,该中性溶液中:c(Cl-)>c(Na+)>c(HCN) |
某醇在适当条件下与足量的乙酸发生酯化,得到的酯的相对分子质量a与原来醇的相对分子量b的关系是a=b+84,有关该醇应该具有的结构特点的描述正确的是( )
| A、该醇分子中一定具有甲基 |
| B、该醇分子中一定没有甲基 |
| C、该醇分子中至少含有三个碳原子 |
| D、该醇分子中具有两个醇羟基 |
下列有关元素周期表的说法中,正确的是( )
| A、能生成碱的金属元素都在ⅠA族 |
| B、原子序数为14的元素位于元素周期表的第3周ⅥA族 |
| C、稀有气体元素原子的最外层电子数为2或8 |
| D、元素周期表有18个纵行,分列16个族,即7个主族、8个副族和1个0族 |
下列表示对应反应的离子方程式正确的是( )
| A、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | ||||
| B、硝酸银溶液中滴加过量氨水:Ag++NH3?H2O═AgOH↓+NH4+ | ||||
C、用惰性电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| D、碳酸氢钠的水解:HCO3-+H2O?CO32-+H3O+ |
将铝条插入盛有CuCl2浓溶液的烧杯,反应过程中一定不可能出现的现象是( )
| A、产生无色气体 |
| B、产生蓝色絮状沉淀 |
| C、紫红色固体析出 |
| D、黄绿色气泡逸出 |
镭是元素周期表中第7周期第ⅡA族元素,下列关于镭的性质描述不正确的是( )
| A、在化合物中呈+2价 |
| B、单质能与水反应放出氢气 |
| C、氢氧化镭比氢氧化钙的碱性弱 |
| D、碳酸镭难溶于水 |