题目内容
某醇在适当条件下与足量的乙酸发生酯化,得到的酯的相对分子质量a与原来醇的相对分子量b的关系是a=b+84,有关该醇应该具有的结构特点的描述正确的是( )
| A、该醇分子中一定具有甲基 |
| B、该醇分子中一定没有甲基 |
| C、该醇分子中至少含有三个碳原子 |
| D、该醇分子中具有两个醇羟基 |
考点:有机物的推断,醇类简介
专题:有机物分子组成通式的应用规律
分析:醇与足量的乙酸反应生成酯,设醇中羟基数目为n,则Mr(醇)+n×Mr(乙酸)=Mr(酯)+n×Mr(水),故Mr(酯)-Mr(醇)=n×Mr(乙酸)-n×Mr(水)=84,即60n-18n=84,解得n=2,据此解答.
解答:
解:醇与足量的乙酸反应生成酯,设醇中羟基数目为n,则Mr(醇)+n×Mr(乙酸)=Mr(酯)+n×Mr(水),故Mr(酯)-Mr(醇)=n×Mr(乙酸)-n×Mr(水)=84,即60n-18n=84,解得n=2,
由于2个-OH连接在同一碳原子上,不稳定,故该醇分子至少有2个C原子,该醇分子中含有2个-OH,故该醇分子中可能含有甲基、也可能没有甲基,综上分析,选项ABC错误,D正确,故选D.
由于2个-OH连接在同一碳原子上,不稳定,故该醇分子至少有2个C原子,该醇分子中含有2个-OH,故该醇分子中可能含有甲基、也可能没有甲基,综上分析,选项ABC错误,D正确,故选D.
点评:本题考查有机物推断,根据酯化反应特点,利用质量守恒确定醇中羟基数目是关键,侧重考查学生对数据的分析处理能力,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列反应的离子方程式正确的是( )
| A、氯气与烧碱溶液反应:Cl2+H2O═Cl-+ClO-+2H+ |
| B、向氯化亚铁溶液中滴入氯水:2Fe2++Cl2═2Fe3++2Cl- |
| C、AlCl3溶液中加入过量的烧碱溶液:Al3++3OH-═Al(OH)3↓ |
| D、小苏打溶液中加入过量的澄清石灰水:Ca2++OH-+HCO3-═CaCO3↓+H2O |
设NA为阿伏加德罗常数,下列说法不正确的是( )
①在铝热反应中,用滤纸做的漏斗必须干燥
②常温常压下,1mol氯气与足量的金属铁反应,转移2NA个电子
③标准状况下,含NA个氧原子的氧单质的体积一定为11.2L
④铅蓄电池中每消耗1mol 硫酸,电路中转移电子数为2NA
⑤将NO2和N2O4分子共NA个降温至标况下,其体积为22.4L
⑥二氧化硅与碳酸钙高温下反应生成二氧化碳,说明硅酸酸性比碳酸强
⑦化学变化不产生新元素,产生新元素的变化不是化学变化.
①在铝热反应中,用滤纸做的漏斗必须干燥
②常温常压下,1mol氯气与足量的金属铁反应,转移2NA个电子
③标准状况下,含NA个氧原子的氧单质的体积一定为11.2L
④铅蓄电池中每消耗1mol 硫酸,电路中转移电子数为2NA
⑤将NO2和N2O4分子共NA个降温至标况下,其体积为22.4L
⑥二氧化硅与碳酸钙高温下反应生成二氧化碳,说明硅酸酸性比碳酸强
⑦化学变化不产生新元素,产生新元素的变化不是化学变化.
| A、①②⑥ | B、①③④⑤⑥ |
| C、③④⑤⑥ | D、②⑤⑥⑦ |
下列叙述正确的是( )
| A、金属氧化物只可能是碱性氧化物或者两性氧化物 |
| B、鸡蛋清中加入硫酸铜溶液会发生盐析现象 |
| C、蔗糖、淀粉、油脂及其水解产物均为非电解质 |
| D、有机分子的结构简式和实验式可能是相同的 |
在V mL Al2(SO4)3溶液中含有Al3+m g,取
mL该溶液用水稀释至4V mL,则SO42-物质的量浓度为( )
| V |
| 4 |
A、
| ||
B、
| ||
C、
| ||
D、
|
某强酸性溶液中,能大量共存的一组是( )
| A、K+、Na+、AlO2-、SO42- |
| B、NH4+、Na+、I-、NO3- |
| C、Na+、K+、SO42-、CO32- |
| D、Mg2+、Al3+、NO3-、SO42- |
有人打算配制下列含有大量四种不同阴、阳离子的溶液,能成功的是( )
| A、H+、Ca2+、Cl-、HCO3- |
| B、Mg2+、Al3+、Cl-、SO42- |
| C、Na+、H+、NO3-、OH- |
| D、NH4+、Ag+、HCO3-、OH- |
能将化学能转化为电能的装置(溶液均为稀硫酸)是( )
A、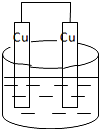 |
B、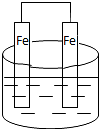 |
C、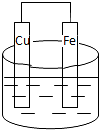 |
D、 |