题目内容
下列表示对应反应的离子方程式正确的是( )
| A、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | ||||
| B、硝酸银溶液中滴加过量氨水:Ag++NH3?H2O═AgOH↓+NH4+ | ||||
C、用惰性电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| D、碳酸氢钠的水解:HCO3-+H2O?CO32-+H3O+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.遵循电子、电荷守恒;
B.滴加过量氨水,生成银氨溶液;
C.电解氯化镁溶液,生成氢氧化镁、氢气、氯气;
D.水解生成碳酸和氢氧根离子.
B.滴加过量氨水,生成银氨溶液;
C.电解氯化镁溶液,生成氢氧化镁、氢气、氯气;
D.水解生成碳酸和氢氧根离子.
解答:
解:A.用过氧化氢从酸化的海带灰浸出液中提取碘的离子反应为2I-+H2O2+2H+═I2+2H2O,故A正确;
B.硝酸银溶液中滴加过量氨水的离子反应为Ag++2NH3?H2O═[Ag(NH3)2]++2H2O,故B错误;
C.用惰性电极电解氯化镁溶液的离子反应为Mg2++2Cl-+2H2O
H2↑+Cl2↑+Mg(OH)2↓,故C错误;
D.碳酸氢钠的水解的离子反应为HCO3-+H2O?H2CO3+OH-,故D错误;
故选A.
B.硝酸银溶液中滴加过量氨水的离子反应为Ag++2NH3?H2O═[Ag(NH3)2]++2H2O,故B错误;
C.用惰性电极电解氯化镁溶液的离子反应为Mg2++2Cl-+2H2O
| ||
D.碳酸氢钠的水解的离子反应为HCO3-+H2O?H2CO3+OH-,故D错误;
故选A.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、水解、电解及氧化还原反应的离子反应考查,综合性较强,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各种溶液中通入足量的SO2后,既无沉淀又无气体产生的有( )种
①Ba(OH)2 ②Ba(NO3)2 ③Na2S ④BaCl2 ⑤Ca(ClO)2 ⑥Fe(NO3)3⑦H2O2 ⑧NaClO ⑨C6H5ONa.
①Ba(OH)2 ②Ba(NO3)2 ③Na2S ④BaCl2 ⑤Ca(ClO)2 ⑥Fe(NO3)3⑦H2O2 ⑧NaClO ⑨C6H5ONa.
| A、3 | B、4 | C、5 | D、6 |
下列叙述正确的是( )
| A、金属氧化物只可能是碱性氧化物或者两性氧化物 |
| B、鸡蛋清中加入硫酸铜溶液会发生盐析现象 |
| C、蔗糖、淀粉、油脂及其水解产物均为非电解质 |
| D、有机分子的结构简式和实验式可能是相同的 |
某强酸性溶液中,能大量共存的一组是( )
| A、K+、Na+、AlO2-、SO42- |
| B、NH4+、Na+、I-、NO3- |
| C、Na+、K+、SO42-、CO32- |
| D、Mg2+、Al3+、NO3-、SO42- |
有人打算配制下列含有大量四种不同阴、阳离子的溶液,能成功的是( )
| A、H+、Ca2+、Cl-、HCO3- |
| B、Mg2+、Al3+、Cl-、SO42- |
| C、Na+、H+、NO3-、OH- |
| D、NH4+、Ag+、HCO3-、OH- |
能将化学能转化为电能的装置(溶液均为稀硫酸)是( )
A、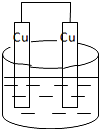 |
B、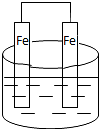 |
C、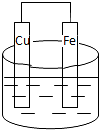 |
D、 |
依据物质的相关数据,可以推断物质的结构和性质.下列利用物质的相关数据作出的相应推断不合理的是( )
| A、依据元素的原子序数,推断该元素原子的核外电子数 |
| B、依据物质相对分子质量,推断物质熔、沸点的高低 |
| C、依据气体的摩尔质量,推断相同状态下不同气体密度的大小 |
| D、依据液体物质的沸点,推断将两种互溶液态混合物用蒸馏法分离的可行性 |
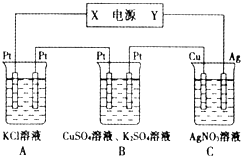 Na-Al/FeS是一种可充电电池,电池中用含Na+导电固体作为电解质,在工作过程中Na+的物质的量保持不变.
Na-Al/FeS是一种可充电电池,电池中用含Na+导电固体作为电解质,在工作过程中Na+的物质的量保持不变.