题目内容
镭是元素周期表中第7周期第ⅡA族元素,下列关于镭的性质描述不正确的是( )
| A、在化合物中呈+2价 |
| B、单质能与水反应放出氢气 |
| C、氢氧化镭比氢氧化钙的碱性弱 |
| D、碳酸镭难溶于水 |
考点:同一主族内元素性质递变规律与原子结构的关系
专题:元素周期律与元素周期表专题
分析:镭是元素周期表中第七周期的ⅡA族元素,最外层有2个电子,性质活泼,易与水反应,利用同主族元素金属性的递变规律分析.
解答:
解:A.镭最外层有2个电子,在化合物中呈+2价,故A正确;
B.同主族元素从上到下金属性逐渐增强,镭的金属性较强,故B正确;
C.同主族元素从上到下金属性逐渐增强,镭的金属性比Ca强,镭的氢氧化物比氢氧化钙的碱性强,故C错误;
D.同主族元素性质相似,碳酸钙不溶于水,则碳酸镭难溶于水,故D正确,
故选C.
B.同主族元素从上到下金属性逐渐增强,镭的金属性较强,故B正确;
C.同主族元素从上到下金属性逐渐增强,镭的金属性比Ca强,镭的氢氧化物比氢氧化钙的碱性强,故C错误;
D.同主族元素性质相似,碳酸钙不溶于水,则碳酸镭难溶于水,故D正确,
故选C.
点评:本题考查同主族元素性质的递变规律,为高频考点,把握同主族元素金属性对应单质、化合物的性质的相似性和递变性为解答的关键,侧重规律性知识的考查,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
某强酸性溶液中,能大量共存的一组是( )
| A、K+、Na+、AlO2-、SO42- |
| B、NH4+、Na+、I-、NO3- |
| C、Na+、K+、SO42-、CO32- |
| D、Mg2+、Al3+、NO3-、SO42- |
依据物质的相关数据,可以推断物质的结构和性质.下列利用物质的相关数据作出的相应推断不合理的是( )
| A、依据元素的原子序数,推断该元素原子的核外电子数 |
| B、依据物质相对分子质量,推断物质熔、沸点的高低 |
| C、依据气体的摩尔质量,推断相同状态下不同气体密度的大小 |
| D、依据液体物质的沸点,推断将两种互溶液态混合物用蒸馏法分离的可行性 |
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项事实不能说明上述观点的是( )
| A、甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使高锰酸钾酸性溶液褪色 |
| B、乙烯能发生加成反应,而乙烷不能发生加成反应 |
| C、苯酚能和氢氧化钠溶液反应,而乙醛不能和氢氧化钠溶液反应 |
| D、苯酚苯环上的氢比苯分子中的氢更容易被卤原子取代 |
除去下列物质中的杂质,所用试剂和方法不正确的是( )
| 物质 | 杂质 | 除杂质所用试剂和方法 | |
| A | KCl溶液 | I2 | CCl4,萃取分液 |
| B | CO2 | HCl | 饱和NaHCO3溶液,洗气 |
| C | FeCl3溶液 | FeCl2 | 过量还原铁粉,过滤 |
| D | Mg粉 | Al粉 | 足量NaOH溶液,过滤 |
| A、A | B、B | C、C | D、D |
下列常见有机物中,既能发生取代反应,又能使溴的CCl4溶液反应褪色的是( )
| A、甲苯 |
B、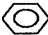 |
| C、植物油 |
| D、CH3COOH |
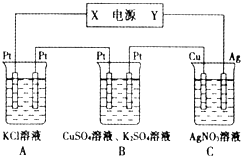 Na-Al/FeS是一种可充电电池,电池中用含Na+导电固体作为电解质,在工作过程中Na+的物质的量保持不变.
Na-Al/FeS是一种可充电电池,电池中用含Na+导电固体作为电解质,在工作过程中Na+的物质的量保持不变.