ƒøƒ⁄»ð
°æƒø°ø»´πÃèÔÆ¡ÚµÁ≥ÿƒÐ¡ø√Ð∂»∏þ°¢≥…±æµÕ£¨∆‰π§◊˜‘≠¿Ì»ÁÕºÀ˘ 棨∆‰÷–µÁº´a≥£”√≤Ù”– ؃´œ©µƒS8≤ƒ¡œ£¨µÁ≥ÿ∑¥”¶Œ™£∫16Li+xS8=8Li2Sx£®2°Ðx°Ð8£©£Æœ¬¡–Àµ∑®¥ÌŒÛµƒ «£®°°°°£©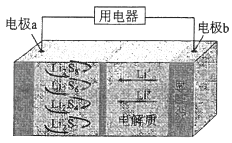
A.µÁ≥ÿπ§◊˜ ±£¨’˝º´ø…∑¢…˙∑¥”¶£∫2Li2S6+2Li++2e©Å=3Li2S4
B.µÁ≥ÿπ§◊˜ ±£¨Õ‚µÁ¬∑÷–¡˜π˝0.02 molµÁ◊”£¨∏∫º´≤ƒ¡œºı÷ÿ0.14 g
C. ؃´œ©µƒ◊˜”√÷˜“™ «Ã·∏þµÁº´aµƒµºµÁ–‘
D.µÁ≥ÿ≥‰µÁ ±º‰‘Ω≥§£¨µÁ≥ÿ÷–µƒLi2S2¡ø‘Ω∂ý
°æ¥∞∏°øD
°æΩ‚Œˆ°øΩ‚£∫A£Ææð∑÷Œˆø…÷™’˝º´ø…∑¢…˙∑¥”¶£∫2Li2S6+2Li++2e©Å=3Li2S4 £¨ π A’˝»∑£ª
B£Æ∏∫º´∑¥”¶Œ™£∫Li©Åe©Å=Li+ £¨ µ±Õ‚µÁ¬∑¡˜π˝0.02molµÁ◊” ±£¨œ˚∫ƒµƒÔÆŒ™0.02mol£¨∏∫º´ºı÷ÿµƒ÷ ¡øŒ™0.02mol°¡7g/mol=0.14g£¨π B’˝»∑£ª
C£Æ¡Ú◊˜Œ™≤ªµºµÁµƒŒÔ÷ £¨µºµÁ–‘∑«≥£≤Ó£¨∂¯ ؃´œ©µƒÃÿ–‘ « “Œ¬œ¬µºµÁ◊Ó∫√µƒ≤ƒ¡œ£¨‘Ú Øƒ´œ©µƒ◊˜”√÷˜“™ «Ã·∏þµÁº´aµƒµºµÁ–‘£¨π C’˝»∑£ª
D£Æ≥‰µÁ ±aŒ™—Ùº´£¨”Î∑≈µÁ ±µƒµÁº´∑¥”¶œý∑¥£¨‘Ú≥‰µÁ ±º‰‘Ω≥§£¨µÁ≥ÿ÷–µƒLi2S2¡øæÕª·‘Ω…Ÿ£¨π D¥ÌŒÛ£ª
π —°D£Æ
”…µÁ≥ÿ∑¥”¶16Li+xS8=8Li2Sx£®2°Ðx°Ð8£©ø…÷™∏∫º´ÔÆ ßµÁ◊”∑¢…˙—ıªØ∑¥”¶£¨µÁº´∑¥”¶Œ™£∫Li©Åe©Å=Li+ £¨ Li+“∆œÚ’˝º´£¨À˘“‘a «’˝º´£¨∑¢…˙ªπ‘≠∑¥”¶£∫S8+2e©Å=S82©Å £¨ S82©Å+2Li+=Li2S8 £¨ 3Li2S8+2Li++2e©Å=4Li2S6 £¨ 2Li2S6+2Li++2e©Å=3Li2S4 £¨ Li2S4+2Li++2e©Å=2Li2S2 £¨ ∏˘æðµÁº´∑¥”¶ ΩΩ·∫œµÁ◊”◊™“∆Ω¯––º∆À„£Æ

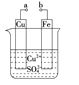
°æƒø°ø¡Ú¥˙¡ÚÀ·ƒ∆»Ð“∫”Îœ°¡ÚÀ·∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™£∫Na2S2O3+H2SO4®TNa2SO4+SO2°¸+S°˝+H2O£¨œ¬¡–∏˜◊È µ—È÷–◊Óœ»≥ˆœ÷ªÎ◊«µƒ «£® £©
µ—È | ∑¥”¶Œ¬∂»/°Ê | Na2S2O3»Ð“∫ | œ°H2S4 | H2O | ||
V/mL | c£®molL©Å1£© | V/mL | c£®molL©Å1£© | V/mL | ||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
A.A
B.B
C.C
D.D
°æƒø°øœ¬±ÌŒ™‘™Àÿ÷Ð∆⁄±Ìµƒ“ª≤ø∑÷£¨”√ªØ—ß”√”Ôªÿ¥œ¬¡–Œ £∫
÷˜◊ ÷Ð∆⁄°° | ¢ÒA | ¢ÚA | ¢ÛA | ¢ÙA | ¢ıA | ¢ˆA | ¢˜A |
1 | ¢Ÿ | ||||||
2 | ¢⁄ | ¢€ | ¢Ð | ||||
3 | ¢ð | ¢Þ | ¢þ | ¢ý | ¢· | ¢‚ |
£®1£©¢ýµƒ‘≠◊”Ω·ππ æ“‚ÕºŒ™________________________________°£
£®2£©¢⁄∫Õ¢€∆¯Ã¨«‚ªØŒÔŒ»∂®–‘µƒ¥Û–°À≥–Ú£∫___________(Ãѧ Ω)°£
£®3£©¢€¢ý¢‚µƒ◊Ó∏þº€∫¨—ıÀ·µƒÀ·–‘◊Ó«øµƒ «__________(Ãѧ Ω)°£
£®4£©¢€µƒ∆¯Ã¨«‚ªØŒÔ”΢€µƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶µƒÀƪ،Ô∑¥”¶…˙≥…µƒ—Œ «________(Ãѧ Ω)£¨À¸ Ù”⁄________(ÃÓ°∞π≤º€ªØ∫œŒÔ°±ªÚ°∞¿Î◊”ªØ∫œŒÔ°±)°£
£®5£©¢Ÿ¢Ð¢‚»˝÷÷‘™Àÿµƒ‘≠◊”ƒÐ–Œ≥…‘≠◊” ˝ƒø±»Œ™1°√1°√1µƒπ≤º€ªØ∫œŒÔ£¨À¸µƒµÁ◊” ΩŒ™________°£
£®6£©”˚±»Ωœ¢Ð∫Õ¢·¡Ω÷÷‘™Àÿµƒ∑«Ω Ù–‘«ø»ı£¨ø…“‘◊˜Œ™—È÷§µƒ÷§æð «________(ÃÓ◊÷ƒ∏)°£
A£Æ±»Ωœ’‚¡Ω÷÷‘™Àÿµ•÷ µƒ∑–µ„
B£Æ±»Ωœ’‚¡Ω÷÷‘™Àÿµ•÷ ”Ϋ‚∆¯ªØ∫œµƒƒ—“◊
C£Æ±»Ωœ’‚¡Ω÷÷‘™Àÿµƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶Àƪ،ԵƒÀ·ºÓ–‘
D£Æ±»Ωœ’‚¡Ω÷÷‘™Àÿµ•÷ ”ÎÀ·ªÚºÓ∑¥”¶µƒƒ—“◊–‘