题目内容
20.下列化学表达方式不正确的是( )| A. | 中子数为20的氯原子:37Cl | B. | Cl-的结构示意图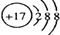 | ||
| C. | 氢氧根离子的电子式: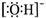 | D. | HClO的结构式 H-Cl-O |
分析 A.质量数=质子数+中子数,元素符号的左上角数字为质量数、左下角数字为质子数;
B.氯离子的核电荷数为17,最外层达到8电子稳定结构;
C.氢氧根离子为带有1个电荷的阴离子,需要标出所带电荷及最外层电子;
D.次氯酸的中心原子为O原子,不存在氢氯键.
解答 解:A.中子数为20的氯原子的质量数为37,该氯原子可以表示为:37Cl,故A正确;
B.Cl-的核外电子总数为18,最外层为8个电子,其离子结构示意图为: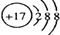 ,故B正确;
,故B正确;
C.氢氧根离子为阴离子,氢氧根离子的电子式为: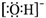 ,故C正确;
,故C正确;
D.次氯酸分子中含有1个氢氧键和1个氧氯键,HClO正确的结构式为:H-O-Cl,故D错误;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、离子结构示意图、结构式、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生规范答题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.将同温同压下H2、O2、Cl2按9:4:1的体积比混合,在密闭容器中用电火花点燃充分反应后,使混合气体冷却到室温,所得溶液的质量分数为( )
| A. | 37% | B. | 33.6% | C. | 16.8% | D. | 20% |
8.下列文字表述与反应方程式对应且正确的是( )
| A. | 实验室制乙炔:CaC2+H2O→Ca(OH)2+C2H2↑ | |
| B. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ | |
| C. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+CO32- | |
| D. | 实验室用液溴和苯在催化剂作用下制溴苯: |
15.下列物质中,互为同位素的是( )
| A. | H2O与D2O | B. | ${\;}_8^{16}O$与${\;}_8^{18}O$ | ||
| C. | 红磷和白磷 | D. | ${\;}_{6}^{12}$C与C60 |
5.同周期的X、Y、Z三元素,其最高价氧化物水化物的酸性由弱到强的顺序是:H3ZO4<H2YO4<HXO4,则下列判断正确的是( )
| A. | 原子半径 X>Y>Z | |
| B. | 非金属性 X>Y>Z | |
| C. | 阴离子的还原性按X、Y、Z的顺序由强到弱 | |
| D. | 气态氢化物的稳定性按X、Y、Z的顺序由弱到强 |
12.三个容器中分别盛有H2、CH4、O2,已知三个容器中气体的温度、密度都相等,下列说法正确的是( )
| A. | 三种气体质量相等 | B. | 三种气体的物质的量之比为16:2:1 | ||
| C. | 三种气体压强比为16:8:1 | D. | 三种气体体积比为1:8:16 |
9.下列说法正确的是( )
| A. | 物质的量是物质粒子的数量的简称 | |
| B. | 摩尔是用来描述物质所含微粒数目多少的基本物理量 | |
| C. | 我们把含有6.02×1023个粒子的任何粒子的集合体计量为1摩尔 | |
| D. | 1mol H2中含2mol电子 |
15.水溶液中下列电离方程式书写正确的是( )
| A. | Ca(OH)2?Ca2++2OH- | B. | NaHCO3═Na++H++CO32- | ||
| C. | H2CO3?2H++CO32- | D. | Na2SO4═2Na++SO42- |