题目内容
15.下列物质中,互为同位素的是( )| A. | H2O与D2O | B. | ${\;}_8^{16}O$与${\;}_8^{18}O$ | ||
| C. | 红磷和白磷 | D. | ${\;}_{6}^{12}$C与C60 |
分析 有相同质子数、不同中子数的原子或同一元素的不同核素互为同位素;
相同元素组成不同形态的单质互为同素异形体.
解答 解:A、H2O、D2O都是水分子,属于同种物质,故A错误;
B、168O和188O质子数相同,中子数不同,互为同位素,故B正确;
C、红磷和白磷均是由磷元素形成的不同单质,互为同素异形体,故C错误;
D、前者为原子,C60为分子,两者均为碳元素形成的微粒,不是同位素,故D错误;
故选B.
点评 本题考查同位素、同素异形体的概念,难度不大,对于元素、核素、同位素、同素异形体、同分异构体、同系物、同种物质等概念的区别是考试的热点问题.

练习册系列答案
相关题目
1.已知在相同温度和压强下,任何气体的分子数之比等于体积比.现有CO、O2、CO2混合气体9mL,点燃爆炸后,恢复到原来状况时,体积减少1mL,再通过足量NaOH溶液体积又减少5mL,则原混合气体中CO、O2、CO2的体积比可能是( )
| A. | 1:3:5 | B. | 5:1:3 | C. | 3:1:5 | D. | 2:4:3 |
9.NA代表阿伏加德罗常数值,下列说法正确的是( )
| A. | 78gNa2O2所含有的离子数为3NA | |
| B. | 1mol甲基中含有电子数为10NA | |
| C. | 7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA | |
| D. | 1molC10H22分子中共价键总数为22NA |
3.下列化学反应的离子方程式不正确的是( )
| A. | Na2S溶液中加入少量FeCl3溶液:2Fe3++S2-═2Fe2++S↓ | |
| B. | 向NaOH溶液中滴加碳酸氢钙溶液至OH-恰好完全反应:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| C. | 向NaClO溶液中通入少量SO2气体:ClO-+SO2+H2O═SO42-+Cl-+2H+ | |
| D. | Na2CO3溶液中滴入少量邻羟基苯甲酸溶液: +CO32-→ +CO32-→ +HCO3- +HCO3- |
10.下列各物质中,互为同系物的是( )
| A. | 式量是16、44、58 的烃 | B. | 所有烯烃 | ||
| C. | C3H4和C4H6 | D. | 乙二醇和丙三醇 |
20.下列化学表达方式不正确的是( )
| A. | 中子数为20的氯原子:37Cl | B. | Cl-的结构示意图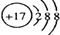 | ||
| C. | 氢氧根离子的电子式: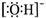 | D. | HClO的结构式 H-Cl-O |
7.原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1.a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同.下列叙述错误的是( )
| A. | a和其他3种元素均能形成共价化合物 | |
| B. | 元素的非金属性次序为c>b>a | |
| C. | d和其他3种元素均能形成离子化合物 | |
| D. | 元素a、b、c各自最高和最低化合价的代数和分别为0、4、6 |
 氯乙烷跟化合物之间的转化如图所示:
氯乙烷跟化合物之间的转化如图所示: