题目内容
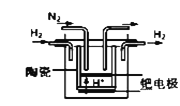
【题目】Ⅰ.甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色。

(1)B中反应的离子方程式是________________________________________________。
(2)为了探究A中溶液由红色变为黄色的原因,甲同学进行如下实验.取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在__________________。
(3)资料显示:SCN -的电子式为 ![]() 。甲同学猜想SCN―可能被Cl2氧化了,他进行了如下研究。①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液, 产生白色沉淀,由此证明SCN―中被氧化的元素是__________________。
。甲同学猜想SCN―可能被Cl2氧化了,他进行了如下研究。①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液, 产生白色沉淀,由此证明SCN―中被氧化的元素是__________________。
②甲同学通过实验证明了SCN―中氮元素转化为NO3―,已知SCN―中碳元素没有被氧化,若SCN―与Cl2反应生成0.5mol CO2,则转移电子的物质的量是_______________mol。
Ⅱ. 8.12天津港特大爆炸事故现场有700吨左右氰化钠,氰化钠剧毒。有少量因爆炸冲击发生泄漏。这些泄露的氰化钠可通过喷洒氧化剂双氧水的方式来处理,以减轻污染。
(1)写出NaCN的电子式__________,偏碱性条件下,氰化钠溶液的CN―被双氧水氧化为HCO3―,同时放出NH3,该反应的离子方程式:____________________________________。
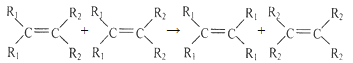
(2)已知CN-离子、SCN-离子和Cl-离子有相似之处,氰分子(CN)2和硫氰分子(SCN)2的性质与Cl2也有相似之处,且常温常压均为气体,完成下列反应方程式:
①MnO2和HSCN的浓溶液共热的化学方程式方式为____________________________。
②(CN)2和NaOH溶液反应的离子反应方程式为_____________________________________。
【答案】 Cl2+2OH―═Cl―+ClO―+H2O Fe3+ 硫元素 8mol Na+[![]() CN﹣+H2O2+H2O═NH3↑+HCO3― MnO2+4HSCN(浓)
CN﹣+H2O2+H2O═NH3↑+HCO3― MnO2+4HSCN(浓)![]() Mn(SCN)2↑+(SCN)2+2H2O (CN)2+2OH-=CN-+CNO-+H2O
Mn(SCN)2↑+(SCN)2+2H2O (CN)2+2OH-=CN-+CNO-+H2O
【解析】Ⅰ.(1)B中反应的离子方程式是Cl2+2OH―═Cl―+ClO―+H2O。
(2)为了探究A中溶液由红色变为黄色的原因,甲同学进行如下实验.取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,该红褐色沉淀为氢氧化铁,说明溶液中一定存在Fe3+。
(3)由资料可知,SCN -的电子式为 ![]() ,其中S为-2价、C为+4价、N为-3价。①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液, 产生白色沉淀,说明溶液中有硫酸根离子,由此证明SCN―中被氧化的元素是硫元素。
,其中S为-2价、C为+4价、N为-3价。①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液, 产生白色沉淀,说明溶液中有硫酸根离子,由此证明SCN―中被氧化的元素是硫元素。
②由题意知,若SCN―与Cl2反应生成0.5mol CO2,则同时生成0.5mol NO3―和0.5mol SO42―,N由-3升高到+5、S由-2升高到+6、C的化合价不变,所以,转移电子的物质的量是8mol。
Ⅱ.(1)NaCN的电子式为Na+[![]() ,偏碱性条件下,氰化钠溶液的CN―被双氧水氧化为HCO3―,同时放出NH3,该反应的离子方程式为CN﹣+H2O2+H2O═NH3↑+HCO3―。
,偏碱性条件下,氰化钠溶液的CN―被双氧水氧化为HCO3―,同时放出NH3,该反应的离子方程式为CN﹣+H2O2+H2O═NH3↑+HCO3―。
(2)①MnO2和HSCN的浓溶液共热,类比MnO2和浓盐酸的反应,该反应的化学方程式方式为MnO2+4HSCN(浓)![]() Mn(SCN)2↑+(SCN)2+2H2O。
Mn(SCN)2↑+(SCN)2+2H2O。
②(CN)2和NaOH溶液反应,类比氯气与NaOH溶液反应,的离子反应方程式为(CN)2+2OH-=CN-+CNO-+H2O。

 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案