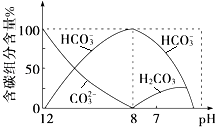
题目内容
【题目】烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1 NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1 SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=_______mol·L-1。
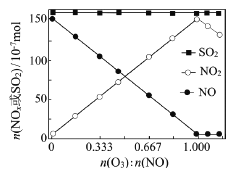
(2)室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见右图。
①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是_________________
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是___________________。
(3)当用CaSO3水悬浮液吸收经O3预处理的烟气时,溶液(pH约为 8)中SO32-将NO2转化为NO2-,其离子方程式为:_________________________________________________________________________________
(4)CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中c(SO32-)=_____________________________[用c(SO42-)、Ksp(CaSO3)和Ksp(CaSO4)表示];CaSO3水悬浮液中加入Na2SO4溶液能提高NO2的吸收速率,其主要原因是__________________________________________________________________
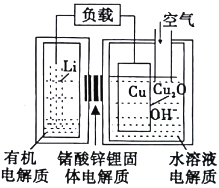
(5)甲醇燃料电池在碱性溶液中的电极反应式。正极_________________________________;负极____________________________________________________________________________
【答案】 -317.3 O3将NO2氧化成更高价氮氧化物 SO2与O3的反应速率慢 SO32-+2NO2+2OH-=SO42-+2NO2-+H2O Ksp(CaSO3)×c(SO42-)/Ksp(CaSO4) CaSO3转化为CaSO4使溶液中SO32-的浓度增大,加快SO32-与NO2的反应速率 3O2 + 6H2O + 12e- = 12OH- 2CH3OH - 12e- + 16OH- = 2CO32- + 12H2O
【解析】(1)设NO(g)+O3(g)=NO2(g)+O2(g) △H1=-200.9kJ·mol-1 ①
NO(g)+1/2O2(g)=NO2(g) △H2=-58.2kJ·mol-1 ②
根据盖斯定律推知,3NO(g)+O3(g)=3NO2(g) △H3=①+2×②=-317.3mol·L-1;
(2)①O3氧化性强,当n(O3):n(NO)>1时,过量的O3可将NO2进一步氧化为更高价氮氧化物(或生成了N2O5);②根据图像可观察到,增加O3的物质的量,SO2的含量变化不大,可能是SO2与O3的反应速率慢,使得O3的含量对该反应的反应速率影响不大。
(3)根据题意,pH约为8的溶液中SO32- 将NO2转化为NO2-,N元素化合价由+4变为+3,被还原,则SO32-被氧化,生成SO42-,根据电子守恒,n(SO32-) :n(NO2)=1:2,可知还需要OH-参与反应,该化学反应方程式为SO32-+2 NO2+2OH-= SO42-+ 2NO2-+H2O;
(4)CaSO3水悬浮液中加入Na2SO4溶液,离子反应方程式为CaSO3+SO42-![]() CaSO4+SO32-,平衡常数,即
CaSO4+SO32-,平衡常数,即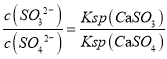 ,故
,故![]() ;根据离子反应方程式可知加入Na2SO4溶液,CaSO3转化为CaSO4使溶液中SO32-的浓度增大,加快SO32-与NO2的反应速率;
;根据离子反应方程式可知加入Na2SO4溶液,CaSO3转化为CaSO4使溶液中SO32-的浓度增大,加快SO32-与NO2的反应速率;
(5)甲醇燃料电池在碱性溶液中的电极反应式,正极:3O2 + 6H2O+12e-=12OH-,负极:2CH3OH-12e-+16OH-= 2CO32-+ 12H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
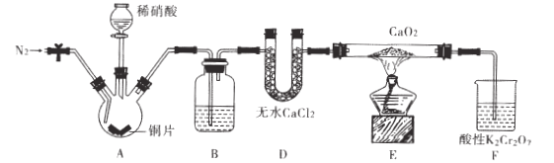
小学生10分钟应用题系列答案【题目】FeCl3是一种常用的净水剂,某化学小组同学用如下装置制备无水FeCl3。已知无水FeCl3在空气中易潮解,加热易升华。请回答下列问题:
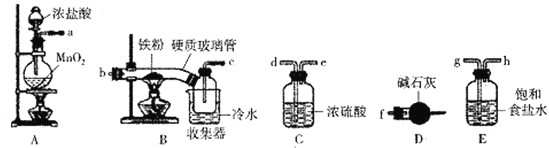
(1)装置A中发生的离子反应方程式为_______________________________。
(2)装置接口的连接顺序为____________ (用a、b、c……h表示)。
(3)装置B中收集器放在冷水中的作用为______________________。
(4)反应结束后,该小组同学对装置B中硬质玻璃管的右端进行加热,其目的是_________________。
(5)反应结束后,该小组同学将装置B中的残留物投入到足量盐酸中溶解.对所得溶液进行如下实验研究,请完成下表实验设计(药品自选)。
实验步骤 | 实验现象 | 实验结论 |
①取少许上述溶液,加入KSCN溶液 | ______ | 含有Fe3+ |
②取少许上述溶液,加入______ | 紫色溶液逐渐变浅至褪色 | _____ |
(6)工业上可用5.0mol·L-1的FeCl3溶液吸收H2S气体,若要吸收170gH2S气体;则需要该FeCl3溶液的体积为____________ mL。