题目内容
2.下图为几种晶体或晶胞的示意图: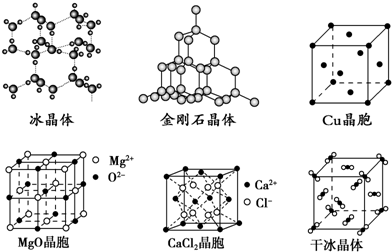
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是金刚石晶体.
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为金刚石、MgO、CaCl2、冰、干冰.
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能小于(填“大于”或“小于”)MgO晶体,原因是MgO晶体中离子的电荷数大于NaCl晶体中离子电荷数,且r(Mg2+)<r(Na+)、r(O2-)<r(Cl-).
(4)每个Cu晶胞中实际占有4个Cu原子,CaCl2晶体中Ca2+的配位数为8.
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是H2O分子之间能形成氢键.
分析 (1)原子晶体中原子间以共价键结合;
(2)熔点的一般规律:原子晶体>离子晶体>分子晶体,同种晶体根据微粒间的作用力大小比较;
(3)离子半径越小,离子带电荷越多,晶格能越大;
(4)Cu原子占据面心和顶点,根据均摊法计算;根据图可知,每个Ca2+周围有8个Cl-,而每个Cl-周围有4个Ca2+;
(5)分子间含有氢键时,其熔沸点较高.
解答 解:(1)原子晶体中原子间以共价键结合,则粒子之间以共价键结合形成的晶体是金刚石晶体;
故答案为:金刚石晶体;
(2)熔点的一般规律:原子晶体>离子晶体>分子晶体,冰和干冰属于分子晶体,熔点:冰>干冰,MgO和CaCl2属于离子晶体,熔点:MgO>CaCl2,金刚石是原子晶体,则熔点由高到低的顺序为:金刚石、MgO、CaCl2、冰、干冰;
故答案为:金刚石、MgO、CaCl2、冰、干冰;
(3)因为MgO中离子带两个电荷,NaCl中离子带一个电荷,氧离子半径小于氯离子,根据离子半径越小,离子带电荷越多,晶格能越大,可得MgO晶体的晶格能大于NaCl晶体的晶格能,
故答案为:MgO晶体中离子的电荷数大于NaCl晶体中离子电荷数,且r(Mg2+)<r(Na+)、r(O2-)<r(Cl-);
(4)Cu原子占据面心和顶点,则每个Cu晶胞中实际占有的原子数为$\frac{1}{8}$×8+$\frac{1}{2}$×6=4;根据氯化钙的晶胞图可知,每个Ca2+周围有8个Cl-,而每个Cl-周围有4个Ca2+,所以
CaCl2晶体中Ca2+的配位数为8;
故答案为:4;8;
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,水分子间含有氢键,氢键的作用力大于范德华力,所以其熔沸点较高;
故答案为:H2O分子之间能形成氢键.
点评 本题考查物质结构与性质,涉及晶体的熔点比较、晶胞结构、晶格能、均摊法在晶胞计算中的应用、氢键等,题目难度中等,解题时要注意基础知识的应用.

| A. | 将LiCoO2改写成为氧化物的形式为Li2O•Co2O3 | |
| B. | 该电池的电解液必须使用有机溶剂主要是由于有机溶剂有良好的导电性 | |
| C. | Li是3号元素,是最轻的金属之一,这类电池质能比高 | |
| D. | 在电池充放电时,Li+在两个电极之间往返嵌入和脱嵌.该电池的充放电反应方程式为:LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6 |
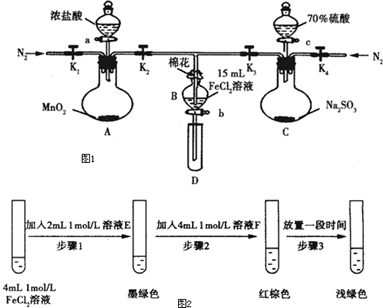
实验过程:
Ⅰ.打开弹簧夹K1~K4,通过一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K2、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K2,活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K2.
Ⅵ.更换试管D,重复过程Ⅳ,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的空气,防止干扰实验.
(2)棉花中浸润的溶液为NaOH溶液.
(3)A中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是70%硫酸中氢离子浓度大于98%的硫酸,因此反应速率更快.
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是乙、丙(填“甲”、“乙”或“丙”).
| 过程Ⅳ:B溶液中含有的离子 | 过程Ⅵ:B溶液中含有的离子 | |
| 甲 | 有Fe3+,无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+、又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+、无Fe2+ | 有Fe2+ |
查阅资料:Fe2+(aq)+2SO32-(aq)?FeSO3(s)(墨绿色)
提出假设:FeCl2与SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色.
某同学设计如图2实验,证实该假设成立:
①溶液E和F分别为Na2SO3、FeCl3.
②请用离子方程式解释步骤3中溶液(酸性)由红棕色变浅绿色的原因Fe3+消耗SO32-,c(SO32-)减小,平衡Fe2+(aq)+SO32-(aq)?FeSO3(s)(墨绿色)逆向移动,溶液颜色由红棕色变为浅绿色.
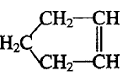 可简写为
可简写为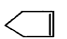 ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为: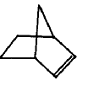
则降冰片烯不具有的性质( )
| A. | 易溶于水 | B. | 能发生氧化反应 | C. | 能发生加成反应 | D. | 能发生取代反应 |
| A. | 2-丙醇 | B. | 2,2-二甲基-1-丙醇 | ||
| C. | 溴乙烷 | D. | 2-甲基-1-丙醇 |
| A. | 钠与水反应 | B. | H+H→H2 | C. | 石灰石分解 | D. | 酸碱中和 |
| A | |||||||||||||||||
| W | T | M | F | ||||||||||||||
| B | D | Z | J | L | H | V | |||||||||||
| C | E | G | Q | ||||||||||||||
(2)属于过渡元素的是G(填字母),H在周期表中的位置第三周期第ⅥA族.
(3)某元素二价阳离子的核外有10个电子,该元素是镁(填元素名称)
(4)L、M、T形成的气态氢化物化合物稳定性由强到弱的顺序H2O>NH3>PH3,J、L、H的最高价氧化物对应水化物的酸性由强到弱的顺序H2SO4>H3PO4>H2SiO3.
(5)D、M、W、E原子半径由大到小的顺序Ca>Mg>C>O.
(6)写出Z单质与B最高价氧化物对应水化物相互反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
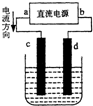
| A. | a为负极、b为正极 | B. | c电极上发生还原反应 | ||
| C. | 电解过程中,d电极质量增加 | D. | 电解过程中,氯离子浓度不变 |
| A. | 氮的非金属性弱 | B. | 氮气的熔沸点低 | ||
| C. | 氮原子半径较小 | D. | 氮分子中原子间共价键不易断裂 |