题目内容
8.下列物质之间的相互关系不正确的是( )| A. | ${\;}_{6}^{12}$C和${\;}_{6}^{14}$C互为同位素 | B. | 02和03互为同素异形体 | ||
| C. |  和 和 互为同分异构体 互为同分异构体 | D. | 干冰和冰为不同种物质 |
分析 A.具有相同质子数,不同中子数(或不同质量数)同一元素的不同核素互为同位素;
B.同种元素形成的不同单质互为同素异形体;
C.具有相同分子式而结构不同的化合物互为同分异构体;
D.同一物质:根据物质的俗名、名称或化学式或主要成分分析判断,主要成分属于同一种物质要求其化学名称相同,化学式相同.
解答 解:A.元素符号左上角的数字为质量数,左下角的数字为质子数,中子数=质量数-质子数,${\;}_{6}^{12}$C和${\;}_{6}^{14}$C质子数都为6,中子数分别为6、8不同,是碳元素的不同原子,互为同位素,故A正确;
B.氧气(O2)与臭氧(O3)都是由氧元素形成的不同单质,互为同素异形体,故B正确;
C. 和
和 都为异丁烷(2-甲基丙烷),属于同一物质,故C错误;
都为异丁烷(2-甲基丙烷),属于同一物质,故C错误;
D.冰是固态的水,其化学式为H2O;干冰是固态的二氧化碳,其化学式为:CO2;不属于同种物质,故D正确;
故选C.
点评 本题考查化学“四同”,题目难度不大,注意把握概念的理解和“四同”间的异同是解决此类题的关键之所在.注意同一物质判别.

练习册系列答案
相关题目
18.(CN)2、(SCN)2等的性质与卤素单质相似,在化学上称为“类卤素”;CN-、SCN-等的性质也与卤离子相似,称为“类卤离子”;不同卤原子能组成卤素互化物,如溴化碘IBr,下面叙述正确的是( )
| A. | (CN)2在碱溶液中生成CN-和OCN- | |
| B. | IBr+2NaOH═NaBr+NaIO+H2O | |
| C. | 均能在空气中燃烧 | |
| D. | IBr与苯发生取代反应生成溴苯和碘化氢 |
3.从11号钠元素到17号氯元素,下列按顺序递减的是( )
| A. | 最外层价电子数 | B. | 原子半径 | C. | 元素的非金属性 | D. | 最高化合价 |
13.下列说法中正确的是( )
| A. | 在原电池中,物质在负极发生氧化反应 | |
| B. | 在原电池中,电子由正极流向负极 | |
| C. | 在电解池中,物质在阴极发生氧化反应 | |
| D. | 在电解池中,与电源正极相连的电极是阴极 |
20.下列关于有机化合物的认识不正确的是( )
| A. | 油脂在空气中完全燃烧转化为水和二氧化碳 | |
| B. | 蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 | |
| C. | 在水溶液里,乙酸分子中的-CH3可以电离出H+ | |
| D. | 医学上了利用银镜反应来检验患者尿液中葡萄糖含量是否偏高 |
 ,它可通过不同化学反应分别制得B、C、D、E四种物质.
,它可通过不同化学反应分别制得B、C、D、E四种物质.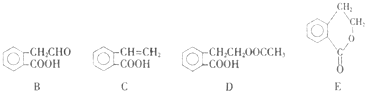
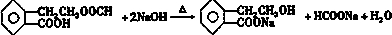 .
.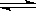 2AB2(g)△H<0,下列说法正确的是( )
2AB2(g)△H<0,下列说法正确的是( ) 2NH3(g) ΔH=-92.4 kJ·m
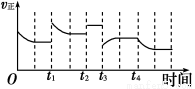
2NH3(g) ΔH=-92.4 kJ·m ol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是
ol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是