题目内容
1.化学实验必须注意安全,下列做法正确的是( )| A. | 制取乙酸乙酯时,先将1体积的酒精倒入3体积的浓硫酸中 | |
| B. | 配置银氨溶液时,将稀氨水滴加到硝酸银溶液中至沉淀恰好溶解为止 | |
| C. | 实验室做钠与乙醇的实验时,余下的钠屑投入到废液缸中 | |
| D. | 制硝基苯时,直接把盛有混合液的试管在酒精灯的外焰处加热 |
分析 A.液体混合时要把密度大的加到密度小的液体中去;
B.配制银氨溶液,最初生成的沉淀恰好溶解即可;
C.金属钠的化学性质很活泼,极易和水发生剧烈反应;
D.制硝基苯时,需要水浴加热.
解答 解:A.浓硫酸的密度大于酒精,应将浓硫酸倒入酒精中,否则会导致混合时产生的大量的热将液体溅出,引发安全事故,故A错误;
B.配制银氨溶液,最初生成的沉淀恰好溶解即可,则在一定量AgNO3溶液中,逐滴滴加稀氨水至沉淀恰好溶解为止,故B正确;
C.金属钠的化学性质很活泼,极易和废液缸中的水发生剧烈反应,引发安全事故,故C错误;
D.制硝基苯时,需要水浴加热50℃~60℃,保证温度恒定,而不能直接在酒精灯火焰上加热,故D错误.
故选B.
点评 本题考查化学实验安全及事故处理,题目难度不大,注意掌握化学实验基本操作方法,明确处理突发事故的方法,确保人身安全、降低国家财产损失.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
16.在372K时,把0.5mol N2O4通入体积为5L的真空密闭容器中,立即出现红棕色.反应进行到2s时,NO2的浓度为0.02mol•L-1.在60s时,体系已达到平衡,此时容器内压强为开始的1.6倍.下列说法正确的是( )
| A. | 前2 s,以N2O4的浓度表示的平均反应速率为 0.01 mol•L-1•s-1 | |
| B. | 在2 s时体系内的压强为开始时的1.1倍 | |
| C. | 在平衡时体系内含N2O40.25 mol | |
| D. | 平衡时,如果压缩容器容积,则可提高N2O4的转化率 |
6.下列事实中,不能用勒夏特列原理加以解释的是( )
| A. | 夏天,打开啤酒瓶时会在瓶口逸出气体 | |
| B. | 浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体 | |
| C. | 压缩氢气与碘蒸气反应的平衡混合气体,颜色变深 | |
| D. | 将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅 |
13.下列各组离子中,相互间不能发生复分解反应的是( )
| A. | Mg2+、NH4+、SO42-、Cl- | B. | Cu2+、Na+、HCO3-、OH- | ||
| C. | K+、Ca2+、NO3-、CO32- | D. | Ag+、Fe3+、Cl-、NO3- |
10.下列叙述正确的是( )
| A. | 1摩尔任何物质都含有6.02×1023个分子 | |
| B. | 摩尔是国际单位制中7个基本物理量之一 | |
| C. | 含有6.02×1023个氧原子的H3PO4的物质的量是0.25mol | |
| D. | 氧气的摩尔质量等于它的相对原子质量 |
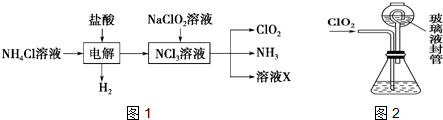
 ,反应A的热化学方程式是4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol.
,反应A的热化学方程式是4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol.