题目内容
下图是一种综合处理SO2废气的工艺流程。下列说法正确的是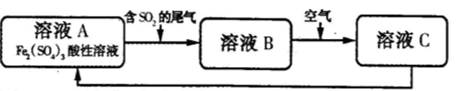
| A.向B溶液中滴加KSCN溶液,溶液变为血红色 |
| B.溶液B转化为溶液C发生的变化的离子方程式为4H++2Fe2++O2=2Fe3++2H2O |
| C.溶液酸性A>B>C |
| D.加氧化亚铁可以使溶液C转化为溶液A |
解析试题分析:A、二氧化硫与铁离子发生氧化还原反应,生成Fe2+,若二氧化硫足量,则溶液中无Fe3+,加入KSCN溶液,溶液不显色;若二氧化硫不足,则溶液变红,正确;B、溶液B中Fe2+被氧气氧化,但电荷不守恒,错误;C、反应由A到B为2H2O + 2Fe3++SO2=2Fe2++ 4H++ SO42-,酸性增强,由B到C溶液酸性减弱,错误;D、氧化亚铁只是溶于酸,不与氯化铁反应,错误。
考点:考查物质的转化有关问题。

练习册系列答案
相关题目
由一种阳离子与两种酸根离子组成的盐称为混盐。混盐CaOCl2在酸性条件下可以产生氯气。该混盐 ( )
| A.水溶液呈中性 |
| B.与硫酸反应产生1mol氯气时转移2mol电子 |
| C.水溶液不能使淀粉-KI试纸变蓝 |
| D.既含离子键又含共价键 |
科技工作者提出用铝粉处理含亚硝酸盐废水的思路:调节亚硝酸盐废水酸碱性,使其pH>12,然后加入适量的铝粉、搅拌,从而实现预期且的。下列判断错误的是
| A.废水处理时铝单质转化为Al3+ | B.废水处理中,亚硝酸盐被还原 |
| C.处理过程中,OH一参与了反应 | D.铝粉颗粒大小影响废水处理的速率 |
下列变化中,必须加入还原剂才能发生的是
| A.FeCl2→FeCl3 | B.H2O→H2 | C.Al→NaAlO2 | D.CO2→C |
下列反应中,氧化剂与还原剂的物质的量之比为1:2的是
①O3+2KI+H2O=2KOH+I2+O2 ②SiO2+2C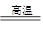 Si+2CO↑
Si+2CO↑
③SiO2+3C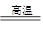 SiC+2CO↑ ④4HCl(浓)+MnO2
SiC+2CO↑ ④4HCl(浓)+MnO2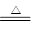 MnCl2+Cl2↑+2H2O( )
MnCl2+Cl2↑+2H2O( )
| A.仅有② | B.②④ | C.②③④ | D.①②③④ |
已知某反应中反应物与生成物有:KIO3、Na2SO3、H2SO4、I2、K2SO4、H2O 和未知物X。下列说法中不正确的是
| A.该未知物X为Na2SO4 |
| B.该反应的氧化剂是KIO3 |
| C.该反应中,发生氧化反应的过程是KIO3→I2 |
| D.由反应可知还原性强弱顺序为:Na2SO3>I2 |
有如下反应:①H2S+H2O2=S↓+2H2O
②S+O2=SO2 ③SO2+Br2+H2O=HBr+H2SO4
下列物质的氧化性强弱判断正确的是( )
| A.H2O2>S O2>SO2 | B.H2O2>O2 Br2>O2 |
| C.Br2>H2O2 SO2>S | D.Br2>H2O2 Br2>SO2 |
氧化还原反应与四种基本反应类型的关系如图所示。下列化学反应属于阴影部分的是( )
| A.2Na2O2+2CO2=2Na2CO3+O2 | B.2NaHCO3=Na2CO3+H2O+CO2↑ |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 | D.Cl2+2KBr=Br2+2KCl |
物质的量之比为1∶3的锌与稀硝酸混合,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,下列说法中正确的是( )
| A.在此反应中硝酸体现强氧化性,全部被还原 |
| B.向反应后的溶液中再加入金属铁,不再发生化学反应 |
| C.该反应中被还原的硝酸与未被还原的硝酸之比为1∶4 |
| D.该反应中被还原的硝酸与未被还原的硝酸之比为1∶5 |