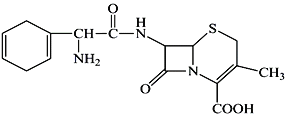
题目内容
【题目】有关下列物质的用途,叙述不正确的是( )
A.氨容易液化,常用作制冷剂
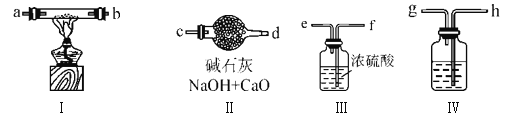
B.浓硫酸可作干燥剂,但不可干燥![]() ,因为浓硫酸具有强氧化性,
,因为浓硫酸具有强氧化性,![]() 具有还原性
具有还原性
C.硅胶可用于袋装食品或药品的干燥剂,也可用作催化剂的载体
D.![]() 均可用于自来水的杀菌、消毒剂,而明矾可作净水剂
均可用于自来水的杀菌、消毒剂,而明矾可作净水剂
【答案】B
【解析】
A. 氨容易液化,液氨气化时吸收大量的热,故常用作制冷剂,A正确;
B. 浓硫酸与![]() 之间不发生氧化还原反应,故浓硫酸可干燥
之间不发生氧化还原反应,故浓硫酸可干燥![]() ,B错误;
,B错误;
C. 硅胶具有吸附性能高、热稳定性好、化学性质稳定、有较高的机械强度等,可用于袋装食品或药品的干燥剂,也可用作催化剂的载体,C正确;
D. ![]() 均因强氧化性可用于自来水的杀菌、消毒剂,而明矾水解产生氢氧化铝胶体可去除水中固体悬浮物,故明矾可作净水剂,D正确;
均因强氧化性可用于自来水的杀菌、消毒剂,而明矾水解产生氢氧化铝胶体可去除水中固体悬浮物,故明矾可作净水剂,D正确;
答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目