题目内容
13.下列表达方式正确的是( )| A. | 碳-12原子:${\;}_{12}^{6}$C | B. | 硫离子结构示意图: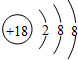 | ||
| C. | 氢氧根的电子式: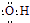 | D. | HClO的结构式:H-O-Cl |
分析 A.元素符号的左上角数字表示的是质量数、左下角数字表示的为质子数;
B.硫原子变成硫离子,核电荷数不变,则硫离子的核电荷数为16;
C.氢氧根离子为阴离子,电子式中需要标出原子的最外层电子及带有的电荷;
D.HClO中存在1个H-O键和1个Cl-O键.
解答 解:A.碳-12的核电荷数为6、质子数为12,该碳原子可以表示为:612C,故A错误;
B.硫离子的核电荷数为16,核外电子总数为18,硫离子正确的结构示意图为: ,故B错误;
,故B错误;
C.氢氧根离子为阴离子,电子式中需要标出电荷及原子的最外层电子,氢氧根离子的电子式为: ,故C错误;
,故C错误;
D.HClO中存在1个H-O键和1个Cl-O键,其结构式为:H-O-Cl,故D正确;
故选D.
点评 本题考查了电子式、元素符号、核外电子排布式的表示方法判断,题目难度中等,注意掌握常见的化学用语的概念及正确的表示方法,明确原子、阴阳离子、离子化合物与共价化合物的电子的区别.

练习册系列答案
相关题目
1.下列反应,既是氧化还原反应又是离子反应的是( )
| A. | 炭在氧气中燃烧 | B. | 二氧化碳通入澄清石灰水中 | ||
| C. | 氯化钠溶液中滴入硝酸银溶液 | D. | 锌粒投入硫酸中 |
8.从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4═3Br2+3Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
| A. | 2NaBr+Cl2═2NaCl+Br2 | |
| B. | AlCl3+3NaAlO2+6H2O═4Al(OH)3↓+3NaCl | |
| C. | 3S+6KOH═2K2S+K2SO3+3H2O | |
| D. | NH4Cl+NaNO2═NaCl+N2↑+2H2O |
18.下列说法正确的是( )
| A. | 90℃时,纯水的pH等于7 | |
| B. | 配制FeCl3溶液,为了抑制水解,常加稀硫酸 | |
| C. | 已知一种c (H+)=1×10-3mol/L的酸和一种c (OH-)=1×10-3mol/L碱溶液以等体积混合后,溶液呈酸性,其原因是浓的弱酸和稀碱反应所致 | |
| D. | 在Na2S溶液中,离子浓度的关系是:c (Na+)>c (S2-)>c (HS-)>c (OH-)>c (H+) |
5.下列说法不正确的是( )
| A. | 煤和石油都是混合物 | |
| B. | 石油通过催化重整可获得环状烃 | |
| C. | 煤的干馏和石油的分馏发生的都是化学变化 | |
| D. | 用溴的四氯化碳溶液可鉴别分馏获得的汽油和裂化获得的汽油 |
2.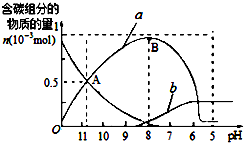 25℃时在10mL 0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
25℃时在10mL 0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
 25℃时在10mL 0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
25℃时在10mL 0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )| A. | Na2CO3溶液中c(Na+)═2[c(CO32-)+c(HCO3-)+c(H2CO3)] | |
| B. | a、b曲线分别代表的是HCO3-、H2CO3量的变化情况 | |
| C. | A点时:c(Na+)>c(CO32-)═c(HCO3-)>c(H+)>c(OH-) | |
| D. | B点时加入盐酸的体积为10mL,两者恰好完全反应生成NaHCO3 |
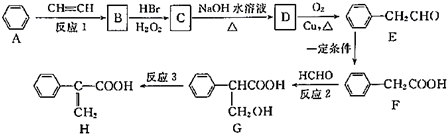
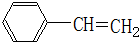 .
. .
.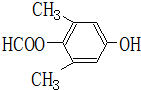 、
、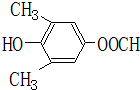 .
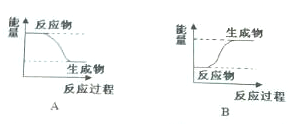
.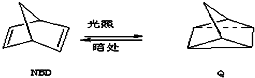 △H=+88.62kJ/mol
△H=+88.62kJ/mol .若用氘(D)原子取代NBD分子中的一个H原子,可得到的同分异构体共有3种.
.若用氘(D)原子取代NBD分子中的一个H原子,可得到的同分异构体共有3种.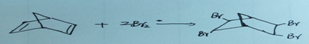 .
.