题目内容
【题目】在以下各种情形下,下列电离方程式的书写正确的是
A.熔融状态下的NaHSO4电离:NaHSO4=Na++H++SO42-
B.H2CO3的电离:H2CO3![]() 2H++CO32-
2H++CO32-
C.Fe(OH)3的电离:Fe(OH)3![]() Fe3++3OH-
Fe3++3OH-
D.水溶液中的NaHSO4电离:NaHSO4=Na++HSO4-
【答案】C
【解析】
试题分析:A.熔融状态下的NaHSO4 电离方程式为NaHSO4=Na++HSO4-,A错误;B.H2CO3的电离分步进行,且以第一步为主,即电离方程式为H2CO3![]() H++HCO3-,B错误;C. Fe(OH)3是多元弱碱,电离一步到位,即 Fe(OH)3
H++HCO3-,B错误;C. Fe(OH)3是多元弱碱,电离一步到位,即 Fe(OH)3 ![]() Fe3++3OH-,C正确;D.水溶液中的 NaHSO4 电离方程式为NaHSO4=Na++H++SO42-,D错误,答案选C。
Fe3++3OH-,C正确;D.水溶液中的 NaHSO4 电离方程式为NaHSO4=Na++H++SO42-,D错误,答案选C。

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案【题目】
(1)写出醋酸在水溶液中的电离方程式 。若某温度下,CH3COOH(aq)与NaOH(aq)反应的△H=" -" 46.8kJ·mol-1,HCl(aq)与NaOH(aq)反应的△H=" -" 55.6 kJ·mol-1,则CH3COOH在水溶液中电离的△H= kJ·mol-1。
(2)某温度下,实验测得0.1mol·L-1醋酸电离度约为1.5%,则该温度下0.1mol·L-1CH3COOH的电离平衡常数K=________(列出计算式,已知电离度![]() )
)
(3)近年来化学家研究开发出用乙烯和乙酸为原料、杂多酸作催化剂合成乙酸乙酯的新工艺,不必生产乙醇或乙醛做中间体,使产品成本降低,具有明显经济优势。其合成的基本反应如下:
![]()
下列描述能说明乙烯与乙酸合成乙酸乙酯的反应已达化学平衡的是 。
A.乙烯、乙酸、乙酸乙酯的浓度相同 |
B.酯化合成反应的速率与酯分解反应的速率相等 |
C.乙烯断开1mol碳碳双键的同时乙酸恰好消耗1mol |
D.体系中乙烯的百分含量一定 |
(4)在n(乙烯)与n(乙酸)物料比为1的条件下,某研究小组在不同压强下进行了在相同时间点乙酸乙酯的产率随温度的变化的测定实验,实验结果如图所示。回答下列问题:
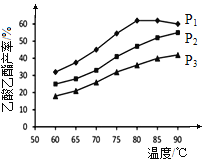
① 温度在60~80℃范围内,乙烯与乙酸酯化合成反应速率由大到小的顺序是 [用![]() (P1)、
(P1)、![]() (P2)、
(P2)、![]() (P3)分别表示不同压强下的反应速率],分析其原因为 。
(P3)分别表示不同压强下的反应速率],分析其原因为 。
②压强为P1MPa、温度60℃时,若乙酸乙酯的产率为30℅,则此时乙烯的转化率为 。
③在压强为P1MPa、温度超过80℃时,乙酸乙酯产率下降的原因可能是_________。
④根据测定实验结果分析,较适宜的生产条件是 (填出合适的压强和温度)。为提高乙酸乙酯的合成速率和产率,可以采取的措施有 (任写出一条)。
【题目】回答有关氯气制备的几个问题
实验室用浓盐酸、二氧化锰共热制氯气,并用氯气和Ca(OH)2制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。现有两个同学分别设计的两套实验装罝如下图:
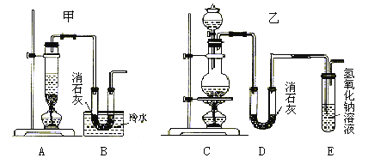
(1)写出制取氯气的离子方程式_______________________________。
(2)请从以下几个方面对甲乙两套实验装置的优缺点作出评价,并将符合题目要求的选项的序号填在表格中。
a.不容易控制反应速率;b.容易控制反应速率;c.有副反应发生;d.可防止副反应发生;e.污染环境;f.可防止污染坏境。
优 点 | 缺点 | |
甲装罝 | ________ | ________ |
乙装罝 | ________ | ________ |
(3)上述装置中甲由A、B两部分组成,乙由C、D、E三部分组成,请从上述装罝中选取合理的部分,组装一套较完整的实验装罝,装置各部分连接顺序是(按气流流动的方向)__________。该组合中还缺少的装罝是_____________,原因是__________________________________。
(4)实验室若用16mol/L的盐酸l00mL与足量的二氧化锰反应,理论上最终生成的次氯酸钙的物质的量最多不超过__________ mol。