��Ŀ����
8���л���A��һ����Ҫ��ҩ�����ʣ�A����Է�������Ϊ166��C��H����Ϊ�ֱ�Ϊ65.1%��6%��A�к������ұ�����ֻ��һ��֧����A��һ�������¿ɷ�������ת��������A��E��Ϊͬ���칹�壬�Ҷ�����̼��������Һ��Ӧ����������̼��F�Ǻ���������Ԫ���Ļ����K��I��������Ӧ�IJ����֪ϩ����һ�������¿ɷ������з�Ӧ��
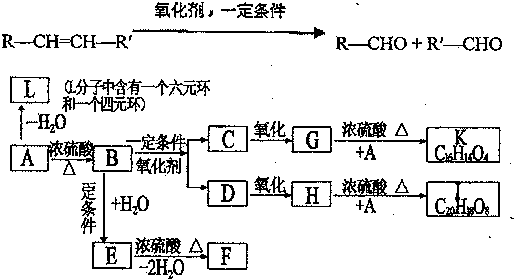
��1��д��A�ķ���ʽC9H10O3��A�����������ŵ����ƴ��ǻ����Ȼ���
��2��д��B��K�Ľṹ��ʽ��B
 ��K
��K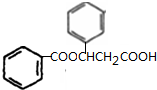 ��
����3��д��A��L�Ļ�ѧ����ʽ
 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$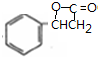 +H2O����Ӧ����ȡ����Ӧ��������Ӧ��
+H2O����Ӧ����ȡ����Ӧ��������Ӧ����4��A��һ��ͬ���칹��M���䱽������������λȡ���������������Ȼ�����Һ������ɫ��Ӧ��M��ϡ���������ˮ������X��Y������Y�����üپ�����ʧ��������������Ԫ�ף���д��M�Ľṹ��ʽ��
 ��
��
���� A��C��HԪ��ԭ�Ӹ����ֱ�Ϊ$\frac{166��65.1%}{12}$=9��$\frac{166��6%}{1}$=10��Oԭ�Ӹ���=$\frac{166����1-65.1%-6%��}{16}$=3��
��A�ķ���ʽΪC9H10O3��A�в����Ͷ�=$\frac{9��2+2-10}{2}$=5�������IJ����Ͷ���4�����Ի�����һ��˫����A�к������ұ�����ֻ��һ��֧����A��һ����������ʧȥһ��ˮ��������L��L�к���һ����Ԫ����һ����Ԫ������A�Ľṹ��ʽΪ ��LΪ
��LΪ ��A��Ӧ����B��B�ܷ��������Ϣ��������Ӧ����B�к���̼̼˫����A������ȥ��Ӧ����B��BΪ
��A��Ӧ����B��B�ܷ��������Ϣ��������Ӧ����B�к���̼̼˫����A������ȥ��Ӧ����B��BΪ ��B��E��ͬ���칹�壬��B��ˮ�����ӳɷ�Ӧ����E��EΪ
��B��E��ͬ���칹�壬��B��ˮ�����ӳɷ�Ӧ����E��EΪ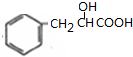 ��Eʧȥ������ˮ����F��F�Ǻ���������Ԫ���Ļ����FΪ
��Eʧȥ������ˮ����F��F�Ǻ���������Ԫ���Ļ����FΪ ��K��I��������Ӧ�IJ��B���ɵ�C��D����ȩ��C��D����������G��H��G��H�����ᣬK�к���16��Cԭ�ӡ�4��Oԭ�ӣ���G��A��1��1��Ӧ����K����CΪ
��K��I��������Ӧ�IJ��B���ɵ�C��D����ȩ��C��D����������G��H��G��H�����ᣬK�к���16��Cԭ�ӡ�4��Oԭ�ӣ���G��A��1��1��Ӧ����K����CΪ ��GΪ
��GΪ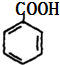 ��DΪOHCCHO��HΪHOOCCOOH��KΪ
��DΪOHCCHO��HΪHOOCCOOH��KΪ ��H��A��1��2��Ӧ����I��IΪ
��H��A��1��2��Ӧ����I��IΪ ���ݴ˷������
���ݴ˷������
��� �⣺A��C��HԪ��ԭ�Ӹ����ֱ�Ϊ$\frac{166��65.1%}{12}$=9��$\frac{166��6%}{1}$=10��Oԭ�Ӹ���=$\frac{166����1-65.1%-6%��}{16}$=3��
��A�ķ���ʽΪC9H10O3��A�в����Ͷ�=$\frac{9��2+2-10}{2}$=5�������IJ����Ͷ���4�����Ի�����һ��˫����A�к������ұ�����ֻ��һ��֧����A��һ����������ʧȥһ��ˮ��������L��L�к���һ����Ԫ����һ����Ԫ������A�Ľṹ��ʽΪ ��LΪ
��LΪ ��A��Ӧ����B��B�ܷ��������Ϣ��������Ӧ����B�к���̼̼˫����A������ȥ��Ӧ����B��BΪ
��A��Ӧ����B��B�ܷ��������Ϣ��������Ӧ����B�к���̼̼˫����A������ȥ��Ӧ����B��BΪ ��B��E��ͬ���칹�壬��B��ˮ�����ӳɷ�Ӧ����E��EΪ
��B��E��ͬ���칹�壬��B��ˮ�����ӳɷ�Ӧ����E��EΪ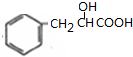 ��Eʧȥ������ˮ����F��F�Ǻ���������Ԫ���Ļ����FΪ
��Eʧȥ������ˮ����F��F�Ǻ���������Ԫ���Ļ����FΪ ��K��I��������Ӧ�IJ��B���ɵ�C��D����ȩ��C��D����������G��H��G��H�����ᣬK�к���16��Cԭ�ӡ�4��Oԭ�ӣ���G��A��1��1��Ӧ����K����CΪ
��K��I��������Ӧ�IJ��B���ɵ�C��D����ȩ��C��D����������G��H��G��H�����ᣬK�к���16��Cԭ�ӡ�4��Oԭ�ӣ���G��A��1��1��Ӧ����K����CΪ ��GΪ
��GΪ ��DΪOHCCHO��HΪHOOCCOOH��KΪ
��DΪOHCCHO��HΪHOOCCOOH��KΪ ��H��A��1��2��Ӧ����I��IΪ
��H��A��1��2��Ӧ����I��IΪ ��
��
��1��A�ķ���ʽΪC9H10O3��A�Ľṹ��ʽΪ ��A�����������ŵ����ƴ��ǻ����Ȼ����ʴ�Ϊ��C9H10O3�����ǻ����Ȼ���
��A�����������ŵ����ƴ��ǻ����Ȼ����ʴ�Ϊ��C9H10O3�����ǻ����Ȼ���
��2��B�Ľṹ��ʽΪ ��K�Ľṹ��ʽΪ
��K�Ľṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
��3��A�Ľṹ��ʽΪ ��LΪ
��LΪ ��A����������Ӧ��ȡ����Ӧ����L����Ӧ������ȡ����Ӧ��������Ӧ����Ӧ����ʽΪ
��A����������Ӧ��ȡ����Ӧ����L����Ӧ������ȡ����Ӧ��������Ӧ����Ӧ����ʽΪ $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$ +H2O��
+H2O��
�ʴ�Ϊ�� $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$ +H2O��ȡ����Ӧ��������Ӧ��
+H2O��ȡ����Ӧ��������Ӧ��
��4��AΪ ��A��һ��ͬ���칹��M���䱽������������λȡ���������������Ȼ�����Һ������ɫ��Ӧ��˵�����з��ǻ���M��ˮ��˵������������Mˮ������X��Y��Y�����üپ�����ʧ��������������Ԫ�ף���YΪCH3OH��YΪ
��A��һ��ͬ���칹��M���䱽������������λȡ���������������Ȼ�����Һ������ɫ��Ӧ��˵�����з��ǻ���M��ˮ��˵������������Mˮ������X��Y��Y�����üپ�����ʧ��������������Ԫ�ף���YΪCH3OH��YΪ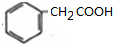 ����MΪ
����MΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ��Լ�֪ʶ�ۺ�Ӧ����������ȷ�ж�A�ṹ��ʽ�ǽⱾ��ؼ����ٽ�Ϸ�Ӧ���������������ʽ��ṹ�ص�����ƶϣ��ѵ���ͬ���칹���жϣ���Ŀ�Ѷ��еȣ�

 ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д� ��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
��Ԫ����ĩ��ϰ�ȷ��ϵ�д�| A�� | ������ | B�� | ������ | C�� | ������ | D�� | ����̼ |
��N2��g��+3H2��g��?2NH3��g����H2=-92.4kJ•mol-1
��2H2��g��+O2��g���T2H2O��g����H3=-483.6kJ•mol-1
����˵����ȷ���ǣ�������
| A�� | �ݷ�Ӧ�ٿ�֪N2��ȼ����Ϊ180 kJ•mol-1 | |
| B�� | 2H2O��l���T2H2��g��+O2��g����H��+483.6 kJ•mol-1 | |
| C�� | ��Ӧ���ں��º����ܱ�������Ӧ��ƽ�����N2��ƽ�������ƶ���������ת���ʼ�С���÷�Ӧ��ƽ�ⳣ������ | |
| D�� | ����֪�����Ĵ��������Ȼ�ѧ����ʽΪ4NH3��g��+5O2��g���T4NO��g��+6H2O��l����H=-906 kJ•mol-1 |
| A�� | ��CH4��NH4+��SO42-Ϊ��������ṹ�����Ʋ�PH4+��PO43-ҲΪ��������ṹ | |
| B�� | NaCl��CsCl��ѧʽ���ƣ���NaCl��CsCl�ľ���ṹҲ���� | |
| C�� | ������ʹ���Ը��������Һ��ɫ���ʱ���ͬϵ��Ҳ����ʹ���Ը��������Һ��ɫ | |
| D�� | CO2ͨ��Ca��ClO��2��Һ����CaCO3��HClO��SO2ͨ��Ca��ClO��2��ҺҲ����CaSO3��HClO |
| A�� | ��ȩ����ȩ | B�� | ��ϩȩ�ͱ���ȩ | C�� | ����ͼ������ | D�� | ��ȩ�������� |
| ʵ�� ���� | G | L | M | R |
| ����ˮ��Ӧ | ��Ӧ | ������Ӧ | δ�� | δ�� |
| ��2mol/L HCl ��Ӧ | �ܽⲢ�ų����� | �ܽⲢ�ų����� | ��Ӧ | ��Ӧ |
| ��Rn+��ˮ��Һ��Ӧ | �ܽⲢ�γɳ��� | δ�� | �ܽⲢ�γɳ��� | δ�� |
| A�� | L��G��R��M | B�� | G��L��M��R | C�� | L��G��M��R | D�� | L��R��G��M |
| A�� | ��֪C��s��+O2��g���TCO2��g����H1��C��s��+$\frac{1}{2}$O2��g���TCO ��g����H2�����H1����H2 | |
| B�� | ��ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l����H=-57.3kJ•mol-1��������0.5molH2SO4��Ũ�����뺬1mol NaOH����Һ��ϣ��ų����ȴ���57.3 kJ | |
| C�� | ��C��ʯī���TC�����ʯ������H=+1.90kJ•mol-1��֪�����ʯ��ʯī�ȶ� | |
| D�� | ��֪�����ı�ȼ����Ϊ-285.8 kJ•mol-1����Ӧ���Ȼ�ѧ����ʽΪ2H2��g��+O2��g��=2H2O��l����H=-285.8kJ•mol-1 |