题目内容
16.类推的思维方法在化学学习与研究中常会产生错误的结论.因此类推出的结论最终要经过实践的检验才能确定其正确与否.下列几种类推结论中正确的是( )| A. | 从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构 | |
| B. | NaCl与CsCl化学式相似,故NaCl与CsCl的晶体结构也相似 | |
| C. | 苯不能使酸性高锰酸钾溶液褪色,故苯的同系物也不能使酸性高锰酸钾溶液褪色 | |
| D. | CO2通入Ca(ClO)2溶液生成CaCO3和HClO,SO2通入Ca(ClO)2溶液也生成CaSO3和HClO |
分析 A.正四面体结构中中心原子价层电子对个数是4,且不含孤电子对;
B.NaCl、CsCl晶胞结构分别为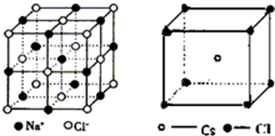 ;
;
C.连接苯环的碳原子上含有H原子的苯的同系物能被酸性高锰酸钾溶液氧化;
D.二氧化硫和次氯酸钙发生氧化还原反应.
解答 解:A.PH4+、PO43-中P原子价层电子对个数都是4且不含孤电子对,所以空间构型为正四面体结构,故A正确;
B.NaCl与CsCl化学式相似,说明两种晶胞中阴阳离子个数比相同,但NaCl、CsCl晶胞结构分别为 ,根据图知,其晶胞结构不同,故B错误;
,根据图知,其晶胞结构不同,故B错误;
C.由于受苯环影响导致连接苯环的烃基较活泼,连接苯环的碳原子上含有H原子的苯的同系物能被酸性高锰酸钾溶液氧化生成苯甲酸而使酸性高锰酸钾溶液褪色,故C错误;
D.二氧化硫具有还原性,次氯酸钙具有强氧化性,二者发生氧化还原反应生成硫酸钙,离子方程式为Ca2++2ClO-+2SO2+2H2O═CaSO4↓+2Cl-+4H++SO42-,故D错误;
故选A.
点评 本题考查探究化学规律,为高频考点,涉及氧化还原反应、苯的同系物的性质、晶胞结构、微粒空间构型判断,明确物质结构、性质及其相互关系即可解答,注意规律中的反常现象,易错选项是CD,注意:只有连接苯环的碳原子上含有H原子的苯的同系物能被酸性高锰酸钾溶液氧化,为易错点.

练习册系列答案
相关题目
6.下列化学式中只能表示一种物质的是( )
| A. | C3H6 | B. | CH2O2 | C. | C2H6O | D. | C3H6O2 |
4.已知化学反应①C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-Q1 kJ/mol②2CO(g)+O2(g)═2CO2(g)△H=-Q2 kJ/mol.据此判断,下列说法正确的是(Q1、Q2均为正数,且其他条件相同)( )
| A. | C的燃烧热为Q1 kJ/mol | |
| B. | 2 mol CO(g)所具有的能量一定高于2 mol CO2(g)所具有的能量 | |
| C. | 一定质量的C燃烧,生成CO2(g)比生成CO(g)时放出的热量多 | |
| D. | C燃烧生成CO2气体的热化学方程式为:C(s)+O2(g)═CO2(g)△H=-(Q1+Q2) kJ/mol |
1.某有机物结构简式如图所示,下列说法正确的是( )
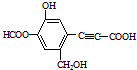

| A. | 该有机物分子式为:C11H10O6 | |
| B. | 分子中最多有9个碳原子共平面 | |
| C. | 该有机物可发生取代反应、还原反应,不能发生银镜反应 | |
| D. | 1 mol该有机物分别与足量Na、NaOH溶液、NaHCO3溶液完全反应,消耗Na、NaOH、NaHCO3的物质的量分别为3mol、4mol、1 mol |
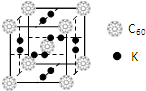 氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.
氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.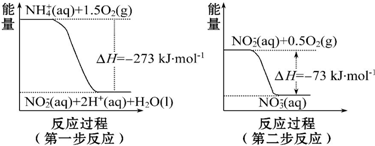
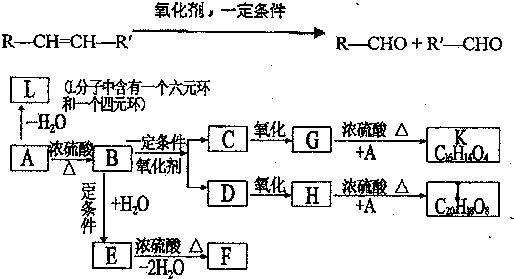
 、K
、K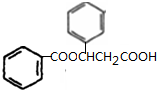 ;
; $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$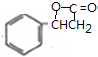 +H2O,反应类型取代反应或酯化反应;
+H2O,反应类型取代反应或酯化反应;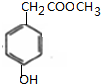 .
.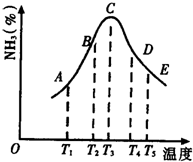 (1)在容积不同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图:
(1)在容积不同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图: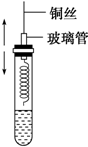 某同学在学习了乙醇的知识后,设计了如图所示的实验.操作步骤及观察到的现象如图:
某同学在学习了乙醇的知识后,设计了如图所示的实验.操作步骤及观察到的现象如图: