题目内容
【题目】锂离子电池己被广泛用作便携式电源。正极材料为LiCoO2、LiFePO4等,负极材料一般为石墨碳,以溶有LiPF6、LiBF4等的碳酸二乙酯(DEC)作电解液。
(1)Fe2+基态核外电子排布式为 ________。
(2)PO43-的空间构型为 ________ (用文字描述)。
(3)![]() 中
中![]() 的配位数为6,该配合物中的配位原子为 _____。
的配位数为6,该配合物中的配位原子为 _____。
(4)碳酸二乙酯(DEC)的分子结构如图所示,分子中碳原子的轨道杂化类型为_____,1mol碳酸二乙酯(DEC)中含有σ键的数目为_____。
![]()
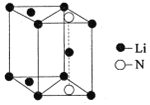
(5)氮化锂是一种新型无机贮氢材料,其晶胞结构如图所示,该晶体的化学式为_______。
【答案】![]() 正四面体 N、Cl sp3、sp2 17NA Li3N
正四面体 N、Cl sp3、sp2 17NA Li3N
【解析】
(1)Fe2+原子核外有24个电子,依据核外电子排布规律, Fe2+基态核外电子排布式为![]() ,
,
故答案为:![]() ;
;
(2)P原子孤电子对数![]() ,价层电子对数
,价层电子对数![]() ,故PO43-的空间构型为正四面体,
,故PO43-的空间构型为正四面体,
故答案为:正四面体;
(3)![]() 中
中![]() 的配位数为6,则配体为Cl和NH3,配位原子为Cl、N,
的配位数为6,则配体为Cl和NH3,配位原子为Cl、N,
故答案为:N、Cl;
(4)根据碳酸二乙酯(DEC)的分子结构示意图可知,碳酸二乙酯中含有酯键,和甲基团,故碳原子的轨道杂化类型为sp3、sp2;碳酸二乙酯中含有17个σ键和一个π键,故1mol碳酸二乙酯(DEC)中含有σ键的数目为17NA,
故答案为:sp3、sp2;17NA;
(5)通过晶胞结构图可知Li原子数![]() ,N原子数
,N原子数![]() ,故化学式为Li3N,
,故化学式为Li3N,
故答案为:Li3N。

练习册系列答案
相关题目