题目内容
12.下列有关实验操作或仪器的使用正确的是( )| A. |  分液时取出下层液体 | B. | 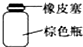 存放浓硝酸 | ||
| C. |  收集NO气体 | D. |  吸收尾气中的SO2 |
分析 A.分液时避免上下层液体混合;
B.浓硝酸有强氧化性;
C.NO能与空气中的氧气反应;
D.二氧化硫能与氢氧化钠反应.
解答 解:A.分液时避免上下层液体混合,则分液时先将下层液体从下口放出,然后上层液体从上口倒出,故A错误;
B.浓硝酸有强氧化性,能氧化橡胶塞,故B错误;
C.NO能与空气中的氧气反应,不能用排空气法收集,故C错误;
D.二氧化硫能与氢氧化钠反应,大肚瓶能防止倒吸,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
相关题目
7.下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是( )
①氯气 ②盐酸 ③新制氯水 ④氯气的酒精溶液 ⑤盐酸酸化的漂白粉溶液.
①氯气 ②盐酸 ③新制氯水 ④氯气的酒精溶液 ⑤盐酸酸化的漂白粉溶液.
| A. | ③⑤ | B. | ③④⑤ | C. | ①②③ | D. | ①③④ |
4.下列变化必须加入还原剂的是( )
| A. | HCO3-→CO2 | B. | KClO3→KCl | C. | FeO→Fe3O4 | D. | MnO4-→Mn2+ |
1.对于平衡CO2(g)═CO2(aq)△H<0,为增大CO2在水中的溶解度,应采用的方法是( )
| A. | 增加压强 | B. | 升高温度 | C. | 不断搅拌 | D. | 升温减压 |
2.能正确表示下列反应的离子方程式( )
| A. | 浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+ | |
| C. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ | |
| D. | 金属铝溶于氢氧化钠溶液:2Al+2OH-+2H2O2[Al(OH)4]-+3H2↑ |
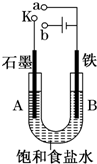 某课外活动小组用如图装置进行实验,试回答下列问题.
某课外活动小组用如图装置进行实验,试回答下列问题. .画出G离子的结构示意图
.画出G离子的结构示意图