题目内容
17.短周期元素A、B、C、D、E、F、G原子序数依次递增,已知A和D,C和G为同一主族元素,D形成的阳离子和C形成的阴离子具有相同的核外电子排布,B原子的最外层电子数比次外层多3,G形成的化合物甲是造成酸雨的主要原因,F和A可形成化合物FA4很不稳定,F与C形成的化合物是制造光导纤维的主要原料,E的最高价氧化物的水化物能溶解于D的最高价氧化物的水化物中.请回答下列问题:(1)写出 E的最高价氧化物水化物的电离方程式AlO2-+H++H2O?Al(OH)3?Al3++3OH-;
(2)由C、D形成的一种淡黄色固体的电子式
 .画出G离子的结构示意图
.画出G离子的结构示意图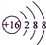
(3)写出E的最高价氧化物的水化物溶解于D的最高价氧化物的水化物的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(4)F和C形成的晶体微粒间的相互作用力是共价键.
(5)化合物甲的治理方法之一是用软锰矿浆(主要成分为MnO2)吸收法,该方法能做到“综合治理、变废为宝”,请写出其反应的化学方程式SO2+MnO2=MnSO4.
(6)已知一包白色晶体为某种正盐,经元素分析仪分析,包含以上七种元素中的若干种,为测定其组成,进行如下实验:
①称取固体2.37g溶于水,得到无色澄清溶液,再滴加过量的氯化钡溶液和稀盐酸,得到的白色沉淀经过滤、洗涤、干燥后,称得质量为4.66g
②再取等质量的该固体溶于水,逐滴滴加1mol/L的氢氧化钠溶液,得到的沉淀和滴加的氢氧化钠溶液体积的关系如图:该正盐的化学式为NH4Al(SO4)2;往该盐的水溶液中滴加氢氧化钡溶液时可得到沉淀,请写出生成沉淀质量达到最大值的离子方程式Al3++NH4++2SO42-+2Ba2++4OH-=Al(OH)3↓+2BaSO4↓+NH3.H2O.
分析 短周期元素A、B、C、D、E、F、G原子序数依次递增,B原子的最外层电子数比次外层多3,原子只能有2个电子层,最外层电子数为5,故B为N元素;F与C形成的化合物是制造光导纤维的主要原料,则C为O元素、F为Si;C和G为同一主族元素,则G为S元素;D形成的阳离子和C(氧)形成的阴离子具有相同的核外电子排布,D处于第三周期,A和D为同一主族元素,F(Si)和A可形成化合物FA4很不稳定,可推知A为H元素、D为Na;D的最高价氧化物的水化物为NaOH,E的最高价氧化物的水化物能溶解与NaOH溶液,E的原子序数介于Na、Si之间,则E为Al,G形成的化合物甲为SO2是造成酸雨的主要原因.
(1)E的最高价氧化物水化物为Al(OH)3,存在酸性电离与碱式电离;
(2)由C、D形成的一种淡黄色固体为Na2O2,由钠离子与过氧根离子构成,G离子为S2-,离子核外有18故电子,有3个电子层,构成电子数为2、8、8;
(3)E的最高价氧化物的水化物为Al(OH)3,D的最高价氧化物的水化物为NaOH,二者反应生成偏铝酸钠与水;
(4)F和C形成的晶体为SiO2,属于原子晶体,微粒间的相互作用力是共价键;
(5)G形成的化合物甲为SO2,与MnO2反应生成MnSO4;
(6)已知一包白色晶体为某种正盐,经元素分析仪分析,包含以上七种元素中的若干种,为测定其组成,进行如下实验:
①称取固体2.37g溶于水,得到无色澄清溶液,再滴加过量的氯化钡溶液和稀盐酸,得到的白色沉淀,则含有SO42-,白色沉淀为BaSO4,其物质的量为$\frac{4.66g}{233g/mol}$=0.02mol,则溶液中n(SO42-)=n(BaSO4)=0.02mol;
②再取等质量的该固体溶于水,逐滴滴加1mol/L的氢氧化钠溶液,开始生成沉淀,最终沉淀完全溶解,则含有Al3+,30mL~40mL时氢氧化铝质量不变,则溶液中还含有NH4+,由Al3++3OH-=Al(OH)3↓可知溶液中n(Al3+)=0.03L×1mol/L×$\frac{1}{3}$=0.01mol,由NH4++OH-=NH3.H2O可知溶液中n(NH4+)=0.01L×1mol/L=0.01mol,符合2n(SO42-)=3n(Al3+)+n(NH4+),而m(SO42-)+m(Al3+)+m(NH4+)=0.02mol×96g/mol/L+0.01mol×27g/mol+0.01mol×18g/mol=2.37g,等于样品的质量,故该晶体不含结晶水,晶体中n(SO42-):n(Al3+):n(NH4+)=0.02mol:0.01mol:0.01mol=2:1:1,故该晶体为NH4Al(SO4)2,
往该盐的水溶液中滴加氢氧化钡溶液时,NH4Al(SO4)2与氢氧化钡按物质的量1:2反应时生成沉淀质量达到最大值.
解答 解:短周期元素A、B、C、D、E、F、G原子序数依次递增,B原子的最外层电子数比次外层多3,原子只能有2个电子层,最外层电子数为5,故B为N元素;F与C形成的化合物是制造光导纤维的主要原料,则C为O元素、F为Si;C和G为同一主族元素,则G为S元素;D形成的阳离子和C(氧)形成的阴离子具有相同的核外电子排布,D处于第三周期,A和D为同一主族元素,F(Si)和A可形成化合物FA4很不稳定,可推知A为H元素、D为Na;D的最高价氧化物的水化物为NaOH,E的最高价氧化物的水化物能溶解与NaOH溶液,E的原子序数介于Na、Si之间,则E为Al,G形成的化合物甲为SO2是造成酸雨的主要原因.
(1)E的最高价氧化物水化物为Al(OH)3,电离方程式为:AlO2-+H++H2O?Al(OH)3?Al3++3OH-,故答案为:AlO2-+H++H2O?Al(OH)3?Al3++3OH-;
(2)由C、D形成的一种淡黄色固体为Na2O2,其电子式为 ,G离子为S2-,离子结构示意图为
,G离子为S2-,离子结构示意图为 ,
,
故答案为: ;
; ;
;
(3)E的最高价氧化物的水化物为Al(OH)3,D的最高价氧化物的水化物为NaOH,二者反应生成偏铝酸钠与水,反应离子方程式:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)F和C形成的晶体为SiO2,属于原子晶体,微粒间的相互作用力是共价键,故答案为:共价键;
(5)G形成的化合物甲为SO2,化合物甲的治理方法之一是用软锰矿浆(主要成分为MnO2)吸收法,该方法能做到“综合治理、变废为宝”,其反应的化学方程式:SO2+MnO2=MnSO4,
故答案为:SO2+MnO2=MnSO4;
(6)已知一包白色晶体为某种正盐,经元素分析仪分析,包含以上七种元素中的若干种,为测定其组成,进行如下实验:
①称取固体2.37g溶于水,得到无色澄清溶液,再滴加过量的氯化钡溶液和稀盐酸,得到的白色沉淀,则含有SO42-,白色沉淀为BaSO4,其物质的量为$\frac{4.66g}{233g/mol}$=0.02mol,则溶液中n(SO42-)=n(BaSO4)=0.02mol;
②再取等质量的该固体溶于水,逐滴滴加1mol/L的氢氧化钠溶液,开始生成沉淀,最终沉淀完全溶解,则含有Al3+,30mL~40mL时氢氧化铝质量不变,则溶液中还含有NH4+,由Al3++3OH-=Al(OH)3↓可知溶液中n(Al3+)=0.03L×1mol/L×$\frac{1}{3}$=0.01mol,由NH4++OH-=NH3.H2O可知溶液中n(NH4+)=0.01L×1mol/L=0.01mol,符合2n(SO42-)=3n(Al3+)+n(NH4+),而m(SO42-)+m(Al3+)+m(NH4+)=0.02mol×96g/mol/L+0.01mol×27g/mol+0.01mol×18g/mol=2.37g,等于样品的质量,故该晶体不含结晶水,晶体中n(SO42-):n(Al3+):n(NH4+)=0.02mol:0.01mol:0.01mol=2:1:1,故该晶体为NH4Al(SO4)2,
往该盐的水溶液中滴加氢氧化钡溶液时,NH4Al(SO4)2与氢氧化钡按物质的量1:2反应时生成沉淀质量达到最大值,反应离子方程式为:Al3++NH4++2SO42-+2Ba2++4OH-=Al(OH)3↓+2BaSO4↓+NH3.H2O,
故答案为:NH4Al(SO4)2;Al3++NH4++2SO42-+2Ba2++4OH-=Al(OH)3↓+2BaSO4↓+NH3.H2O.
点评 本题考查结构性质位置关系应用、无机物推断等,侧重考查学生分析推理能力、知识迁移运用能力,(6)中关键是根据反应判断溶液中含有的离子,难度中等.

| A. | 同温同压下,相同体积的物质,它们的物质的量必相等 | |
| B. | 任何条件下,等物质的量的N2和CO所含的分子数必相等 | |
| C. | 1L一氧化碳气体一定比1L氧气的质量小 | |
| D. | 铁的摩尔质量在数值上等于铁原子的相对原子质量 |
| A. |  分液时取出下层液体 | B. | 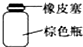 存放浓硝酸 | ||
| C. |  收集NO气体 | D. |  吸收尾气中的SO2 |
| A. | $\frac{n(A-N+8)}{A+16}$mol | B. | $\frac{n(A-N+2)}{A}$ mol | C. | $\frac{n(A-N+8)}{A+8}$mol | D. | $\frac{n(A-N-2)}{A}$ mol |
| A. | CH3CH3,C2H6 | B. | -NO2,NO2 | C. |  ,OH- ,OH- | D. | 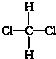 , ,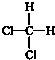 |
 如表中的数据是破坏1mol物质的化学键所消耗的能量:
如表中的数据是破坏1mol物质的化学键所消耗的能量:| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 431 | 366 | 298 | 436 |
(1)下列氢化物中,最不稳定的是C
A.HCl B.HBr C.HI
(2)H2和Cl2反应生成HCl过程中的热效应可用图表示,请回答下列问题:
①△H1=+243kJ•mol-1,△H2=+436kJ•mol-1,△H3=-431kJ•mol-1.
②据实验测定,H2和Cl2的混合气体在光照下反应生成HCl,引发该反应的步骤是上图①~③中分子转化为原子的一步,你认为是第①(填序号)步,请说明原因:Cl-Cl键的键能比H-H键的键能小,更易断裂,从而引发反应.
③该反应的热化学方程式为H2(g)+Cl2(g)=2HCl(g)△H=-183kJ•mol-1.