题目内容
2.在下列元素中,不属于主族元素的是( )| A. | 氢 | B. | 钙 | C. | 铁 | D. | 碘 |
分析 A、氢位于周期表中第一周期A族;
B、钙位于周期表中第四周期ⅡA族;
C、铁周期表中第四周期ⅤⅢ族;
D、碘铁周期表中第五周期ⅤⅡA族.
解答 解:A、氢位于周期表中第一周期A族,故A不选;
B、钙位于周期表中第四周期ⅡA族,故B不选;
C、铁周期表中第四周期ⅤⅢ族,故C选;
D、碘铁周期表中第五周期ⅤⅡA族,故D不选;
故选:C.
点评 本题主要考查了元素在周期表中的位置,学生应根据元素在周期表中的位置综合解答,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.如图,a、b、c、d均为石墨电极,下列说法正确的是( )
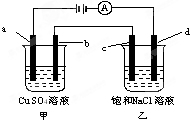

| A. | 甲烧杯中溶液的pH增大,乙烧杯中溶液的pH减小 | |
| B. | 甲烧杯中a电极发生氧化反应,电极反应式为:4OH--4e-═O2↑+2H2O | |
| C. | 电解一段时间后,b极质量增加,c极附近滴加酚酞溶液变红 | |
| D. | C是阳极,电子从d电极通过溶液流向c电极 |
10. 先进的高能量密度二次电池对下一代电动汽车的发展和可再生能源发电的有效利用具有至关重要的作用.室温Al-Mn2O4二次电池是一种新型电池,由Al3+、Al2Cl7和${AlCl}_{4}^{-}$组成的离子液体为该电池的电解液,电池结构如图所示,放电时的总反应式为Al+Mn2O4═AlMn2O4.下列说法正确的是( )
先进的高能量密度二次电池对下一代电动汽车的发展和可再生能源发电的有效利用具有至关重要的作用.室温Al-Mn2O4二次电池是一种新型电池,由Al3+、Al2Cl7和${AlCl}_{4}^{-}$组成的离子液体为该电池的电解液,电池结构如图所示,放电时的总反应式为Al+Mn2O4═AlMn2O4.下列说法正确的是( )
 先进的高能量密度二次电池对下一代电动汽车的发展和可再生能源发电的有效利用具有至关重要的作用.室温Al-Mn2O4二次电池是一种新型电池,由Al3+、Al2Cl7和${AlCl}_{4}^{-}$组成的离子液体为该电池的电解液,电池结构如图所示,放电时的总反应式为Al+Mn2O4═AlMn2O4.下列说法正确的是( )
先进的高能量密度二次电池对下一代电动汽车的发展和可再生能源发电的有效利用具有至关重要的作用.室温Al-Mn2O4二次电池是一种新型电池,由Al3+、Al2Cl7和${AlCl}_{4}^{-}$组成的离子液体为该电池的电解液,电池结构如图所示,放电时的总反应式为Al+Mn2O4═AlMn2O4.下列说法正确的是( )| A. | 放电时,负极的电池反应式为AlMn2O4-3e-═Mn2O4+Al3+ | |
| B. | 放电时,Al3+向负极移动 | |
| C. | 充电时,Mn2O4极与电源的负极相连 | |
| D. | 充电时,Al电极质量增加 |
7.下列离子方程式书写正确的是( )
| A. | 向Fe(NO3)2稀溶液中加入盐酸:Fe2++2H+═3Fe2++H2↑ | |
| B. | 铜片放入稀硝酸中:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH-═NH3↑+H2O | |
| D. | AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
14.含有SiO2的黄铁矿试样1克,在O2中充分灼烧后残余固体为0.76克(设反应过程有2%的硫损失),用这种黄铁矿100吨可制得98%的浓硫酸的质量( )
| A. | 120吨 | B. | 117.6吨 | C. | 116吨 | D. | 121吨 |
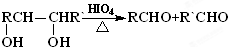
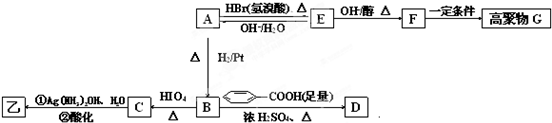
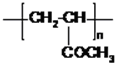 ;
;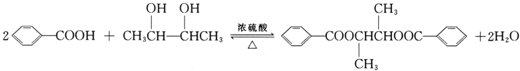 ;
;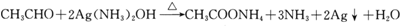 .
.